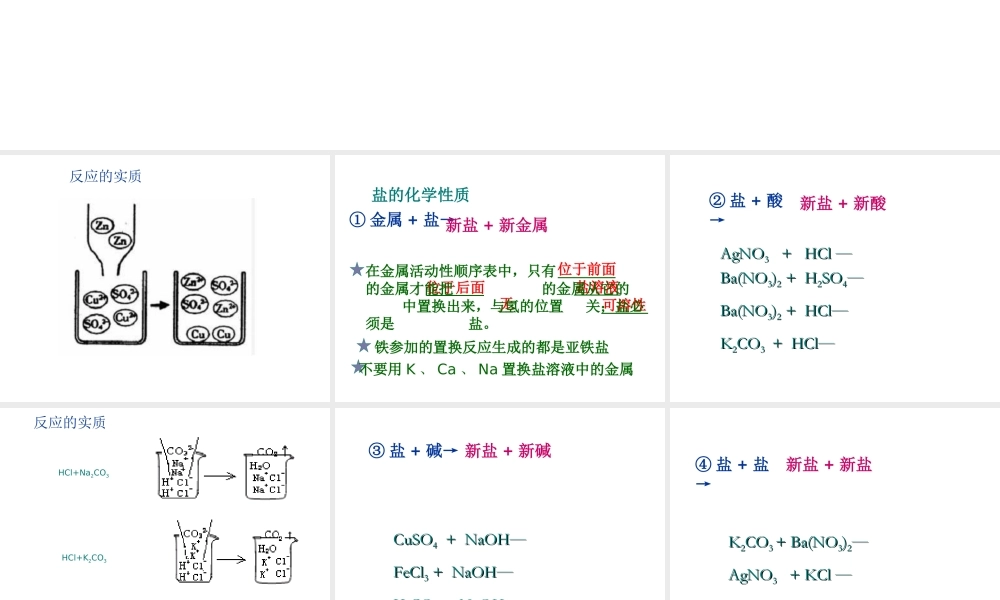
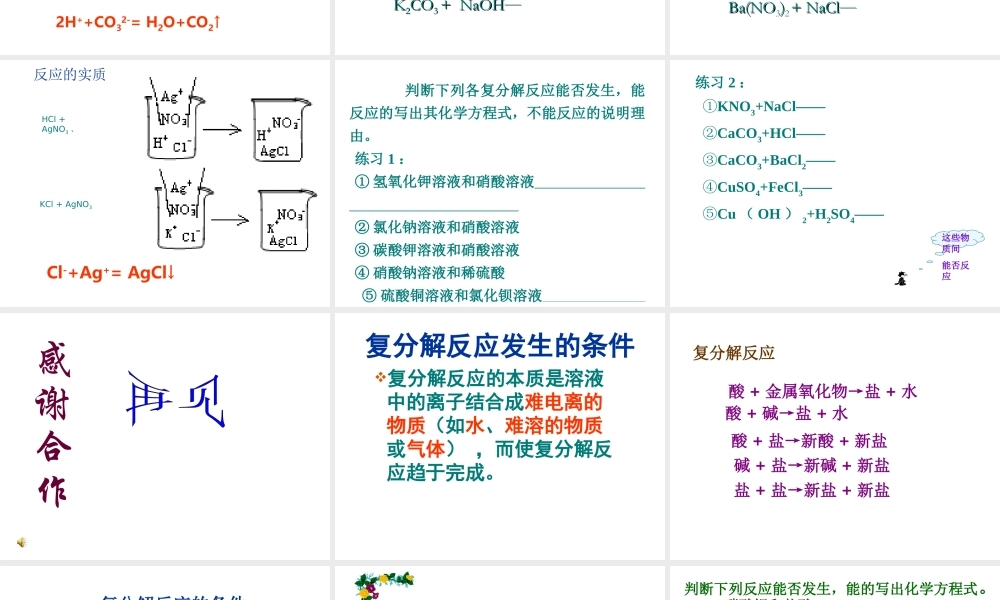
反应的实质盐的化学性质① 金属 + 盐→新盐 + 新金属位于前面位于后面盐溶液无可溶性在金属活动性顺序表中,只有 的金属才能把 的金属从它的 中置换出来,与氢的位置 关;盐必须是 盐
不要用 K 、 Ca 、 Na 置换盐溶液中的金属铁参加的置换反应生成的都是亚铁盐② 盐 + 酸→新盐 + 新酸AgNOAgNO33 + HCl ─ + HCl ─Ba(NOBa(NO33))22 + H + H22SOSO44──Ba(NOBa(NO33))22 + HCl─ + HCl─KK22COCO3 3 + HCl─+ HCl─反应的实质HCl+Na2CO32H++CO32-= H2O+CO2↑HCl+K2CO3 ③ 盐 + 碱→ 新盐 + 新碱CuSOCuSO44 + NaOH─ + NaOH─FeClFeCl33 + NaOH─ + NaOH─KK22COCO3 3 + NaOH─+ NaOH─④ 盐 + 盐→新盐 + 新盐KK22COCO3 3 + Ba(NO+ Ba(NO33))22──AgNOAgNO33 + KCl ─ + KCl ─Ba(NOBa(NO3))2 + NaCl─+ NaCl─HCl + AgNO3 、Cl-+Ag+= AgCl↓反应的实质KCl + AgNO3 判断下列各复分解反应能否发生,能反应的写出其化学方程式,不能反应的说明理由
练习 1 :① 氢氧化钾溶液和硝酸溶液 ② 氯化钠溶液和硝酸溶液③ 碳酸钾溶液和硝酸溶液④ 硝酸钠溶液和稀硫酸 ⑤ 硫酸铜溶液和氯化钡溶液 练习 2 : ①KNO3+NaCl—— ②CaCO3+HCl—— ③CaCO3+BaCl2—— ④CuSO4+FeCl3—— ⑤Cu ( OH ) 2+H2SO4——这些物质间能否反应感谢合作复分解反应发生的条件复分解反应的本质是溶液中的离子结合成难电离的物质(如水、难溶的物质或气体)