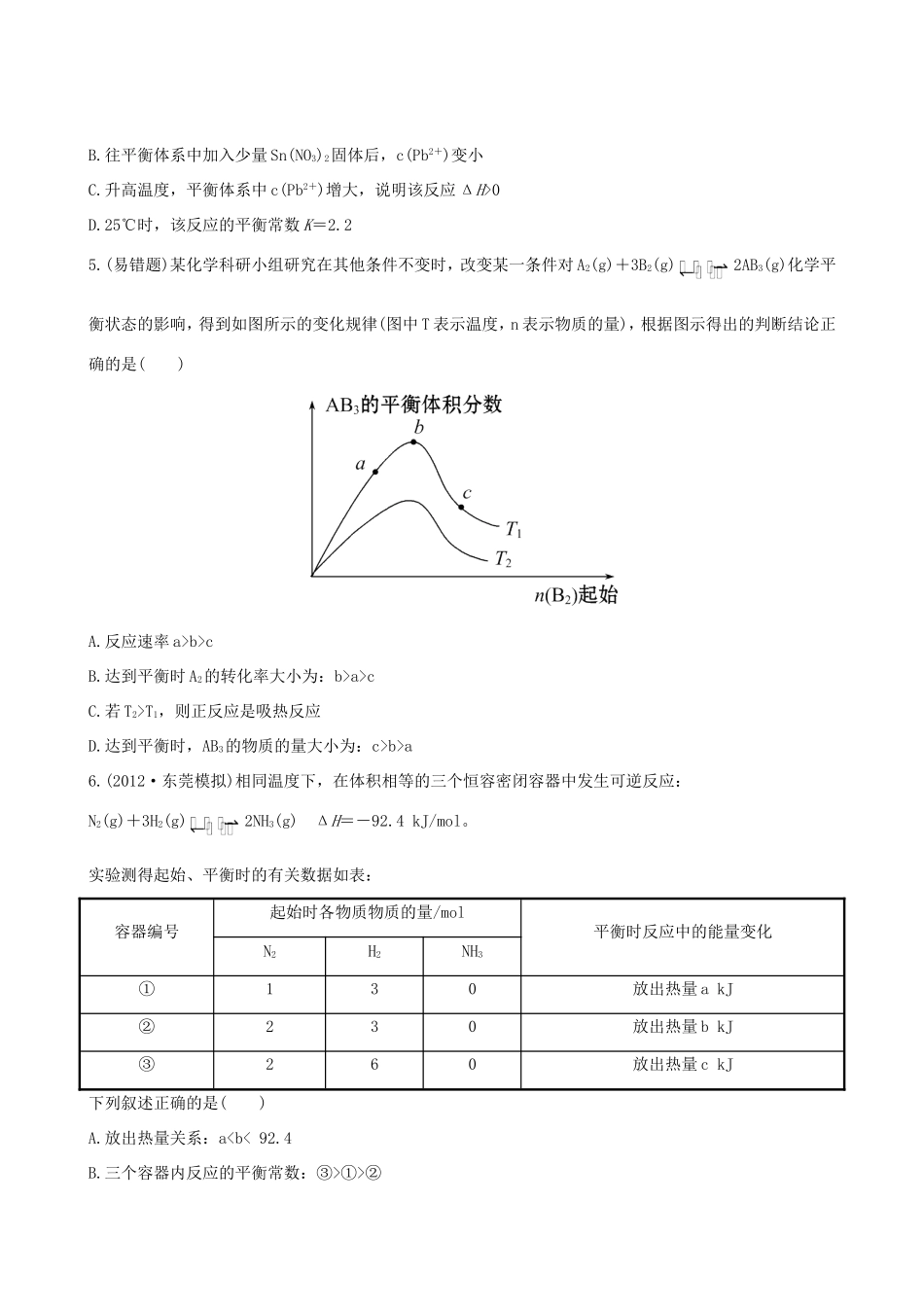
(45分钟100分)一、单项选择题(本大题共8小题,每小题5分,共40分。在每小题给出的四个选项中,只有一个选项符合题目要求)1.(2011·江苏高考改编)下列说法正确的是()A.一定温度下,反应MgCl2(l)===Mg(l)+Cl2(g)的ΔH<0ΔS>0B.水解反应NH+H2ONH3·H2O+H+达到平衡后,升高温度平衡逆向移动C.铅蓄电池放电时的负极和充电时的阳极均发生还原反应D.对于反应2H2O2===2H2O+O2↑,加入MnO2或升高温度都能加快O2的生成速率2.某温度下,可逆反应mA(g)+nB(g)pC(g)+qD(g)平衡常数为K,下列说法正确的是()A.K越大,达到平衡时,反应进行的程度越大B.K随着温度的升高而增大C.K越小,达到平衡时,反应物的转化率越大D.K随反应物浓度的改变而改变3.下列叙述不正确的是()A.化学平衡发生移动,平衡常数不一定发生变化B.升高温度会增大化学反应速率,其原因是增大了活化分子的百分数C.某化学反应的能量变化如图所示,则该反应的ΔH>0,ΔS>0D.H3PO4的电离常数:K1K2K34.(2011·福建高考)25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn(s)+Pb2+(aq)Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示。下列判断正确的是()A.往平衡体系中加入少量金属铅后,c(Pb2+)增大B.往平衡体系中加入少量Sn(NO3)2固体后,c(Pb2+)变小C.升高温度,平衡体系中c(Pb2+)增大,说明该反应ΔH>0D.25℃时,该反应的平衡常数K=2.25.(易错题)某化学科研小组研究在其他条件不变时,改变某一条件对A2(g)+3B2(g)2AB3(g)化学平衡状态的影响,得到如图所示的变化规律(图中T表示温度,n表示物质的量),根据图示得出的判断结论正确的是()A.反应速率a>b>cB.达到平衡时A2的转化率大小为:b>a>cC.若T2>T1,则正反应是吸热反应D.达到平衡时,AB3的物质的量大小为:c>b>a6.(2012·东莞模拟)相同温度下,在体积相等的三个恒容密闭容器中发生可逆反应:N2(g)+3H2(g)2NH3(g)ΔH=-92.4kJ/mol。实验测得起始、平衡时的有关数据如表:容器编号起始时各物质物质的量/mol平衡时反应中的能量变化N2H2NH3①130放出热量akJ②230放出热量bkJ③260放出热量ckJ下列叙述正确的是()A.放出热量关系:a①>②C.达到平衡时氨气的体积分数:①>③D.N2的转化率:②>①>③7.已知:2CH3OH(g)CH3OCH3(g)+H2O(g)ΔH=-25kJ/mol某温度下的平衡常数为400。此温度下,在1L的密闭容器中加入CH3OH,反应到某时刻测得各组分的物质的量浓度如下:物质CH3OHCH3OCH3H2Oc/(mol·L-1)0.81.241.24下列说法正确的是()①平衡后升高温度,平衡常数>400②平衡时,c(CH3OCH3)=1.6mol/L③平衡时,反应混合物的总能量减少20kJ④平衡时,再加入与起始等量的CH3OH,达新平衡后CH3OH转化率增大⑤此时刻反应达到平衡状态⑥平衡时CH3OH的浓度为0.08mol·L-1A.①②④⑤B.②⑥C.②③④⑥D.②④⑥8.(预测题)FeCl3(aq)与KSCN(aq)混合时存在下列平衡:Fe3+(aq)+SCN-(aq)Fe(SCN)2+(aq)。已知平衡时,物质的量浓度c[Fe(SCN)2+]与温度T的关系如图所示,则下列说法正确的是()A.FeCl3(aq)与KSCN(aq)反应的热化学方程式为:Fe3+(aq)+SCN-(aq)===Fe(SCN)2+(aq)ΔH>0B.温度为T1、T2时,反应的平衡常数分别为K1、K2,则K1v(逆)D.A点与B点相比,A点的c(Fe3+)大二、双项选择题(本大题共2小题,每小题6分,共12分。在每小题给出的四个选项中,有两个选项符合题目要求)9.(2012·深圳模拟)某恒温密闭容器发生可逆反应Z(?)+W(?)X(g)+Y(?)ΔH,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件。下列有关说法中不正确的是()A.Z和W在该条件下一定不为气态B.t1~t2时间段与t3时刻后,两时间段反应体系中气体的平均摩尔质量不可能相等C.若在该温度下此反应平衡常数表达式为K=c(X),则t1~t2时间段与t3时刻后的X浓度相等D.若该反应只在某温度T0以上自发进行,则该反应的平衡常数K随温度升高而减小10.(2011·江苏高考)700℃时,向容积为2L的密闭容器中充入一定量的CO和H2O,发生反应:CO(g)+H2O(g)CO2(g)+H2(g),反应过程中测...