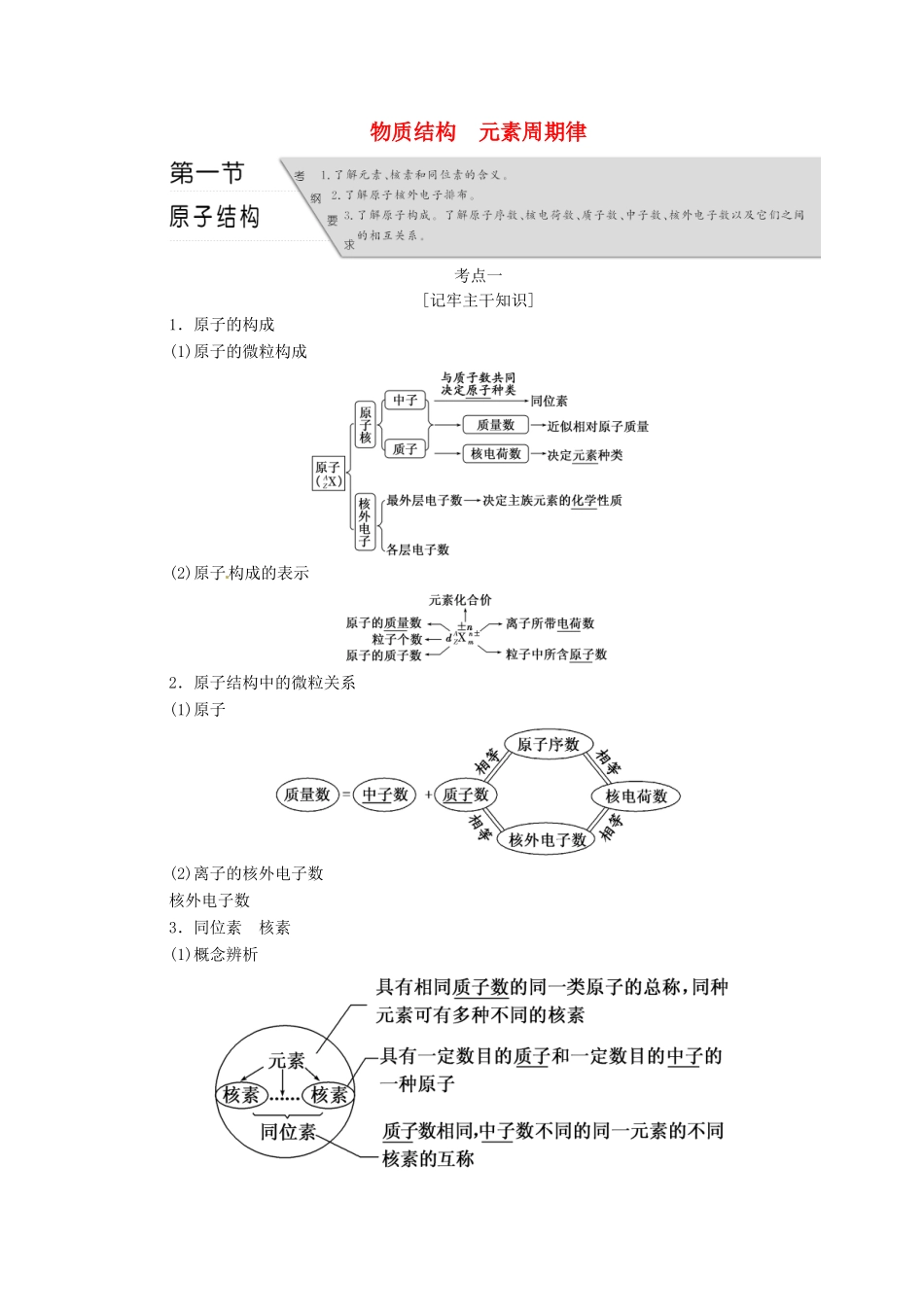
物质结构元素周期律考点一[记牢主干知识]1.原子的构成(1)原子的微粒构成(2)原子构成的表示2.原子结构中的微粒关系(1)原子(2)离子的核外电子数核外电子数3.同位素核素(1)概念辨析(2)同位素的特征①相同存在形态的同位素,化学性质几乎完全相同,物理性质不同
②天然存在的同一元素各核素所占的原子百分数一般不变
(3)常见的重要核素及其应用核素UCHHO用途核燃料用于考古断代制氢弹示踪原子[练通基础小题]一、基础知识全面练1.判断正误(正确的打“√”,错误的打“×”)
(1)所有的原子中都含有质子和中子(×)(2)34S原子核内中子数为16(×)(3)2H+核外电子数为2(×)(4)13C和15N核内中子数相差1(√)(5)H3O+和OH-中具有相同的质子数和电子数(×)(6)1HO的摩尔质量为20g·mol-1(√)(7)质量数就是元素的相对原子质量(×)(8)质子数相同的粒子一定属于同一种元素(×)(9)一种单质中可能含有多种核素,如O2中含16O、17O、18O三种核素(√)(10)H+、H+和H+互称同位素(×)2.(1)在6Li、7Li、23Na、24Mg、14C、14N六种粒子中,包含______种元素,________种核素,其中互为同位素的是________,中子数相等的核素是__________
(2)D3O+中的质子数为________,电子数为________,中子数为________
答案:(1)566Li与7Li23Na与24Mg(2)111011二、常考题点分组练题点(一)原子的表示方法及各微粒数目之间的关系1.下列说法正确的是()A.(2015·全国卷Ⅱ)235g核素U发生裂变反应:U+n――→Sr+Xe+10n,净产生的中子(n)数为10NAB.(2014·山东高考)Cl与Cl得电子能力相同C.(2013·江苏高考)中子数为146、质子数