微考点60弱电解质的电离平衡一、平衡移动,结果判断1.某温度下,相同pH的盐酸和醋酸溶液分别加水稀释,溶液pH随溶液体积变化的曲线如右图所示
据图判断下列说法正确的是()A.Ⅱ为盐酸稀释时的pH变化曲线B.b点溶液的导电性比c点溶液的导电性强C.a点Kw的数值比c点Kw的数值大D.b点酸的总浓度大于a点酸的总浓度2.(2017·徐州模拟)对常温下pH=3的CH3COOH溶液,下列叙述不正确的是()A.c(H+)=c(CH3COO-)+c(OH-)B.加入少量CH3COONa固体后,c(CH3COO-)降低C.该溶液中由水电离出的c(H+)是1
0×10-11mol·L-1D.与等体积pH=11的NaOH溶液混合后所得溶液显酸性二、强化比较,全面认识3.25℃,两种酸的电离常数如下表
Ka1Ka2H2A1
3×10-26
3×10-6H2B4
2×10-75
6×10-7下列叙述中正确的是()A.H2A的电离方程式:H2A===2H++A2-B.常温下,在水中Na2B的水解平衡常数为Ka1=C.等浓度的Na2A和Na2B溶液,由水电离产生的H+浓度大小关系:前者大于后者D.向Na2B溶液中加入少量H2A溶液,可发生反应:B2-+H2A===A2-+H2B4.高氯酸、硫酸、硝酸和盐酸都是强酸,其酸性在水溶液中差别不大
以下是某温度下这4种酸在冰醋酸中的电离常数:酸HClO4H2SO4HClHNO3Ka1
6×10-56
3×10-91
6×10-94
2×10-10从以上表格中判断以下说法不正确的是()A.在冰醋酸中这4种酸都完全电离B.在冰醋酸中高氯酸是这4种酸中最强的酸C.在冰醋酸中硫酸的电离方程式为H2SO4===2H++SOD.水对于这4种酸的强弱没有区分能力,但醋酸可以区别这4种酸的强弱5.将0
1mol·L-1氢氧化钠溶液滴入等体积、浓度均为0
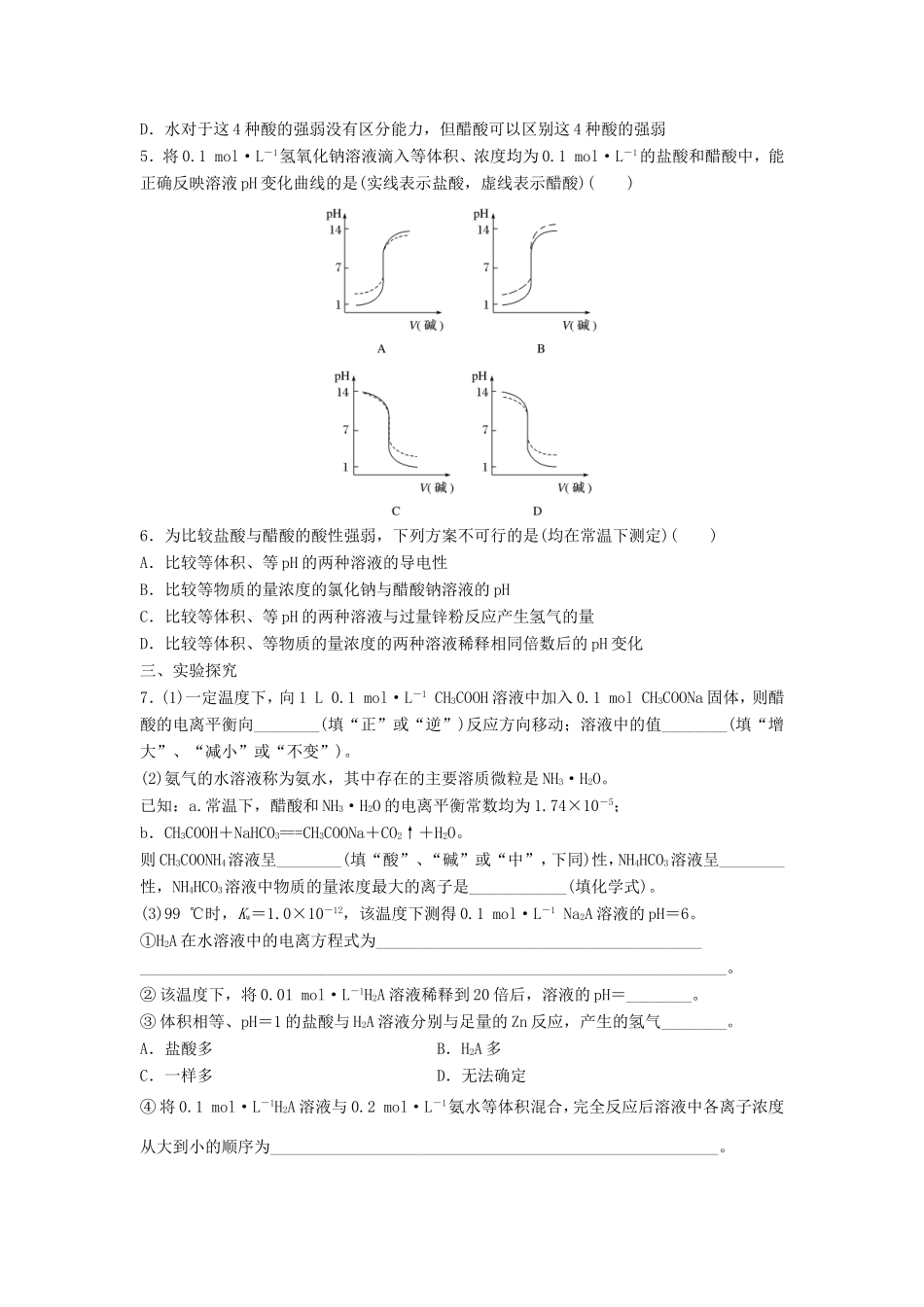
1mol·L-1的盐