北京龙文环球教育科技有限公司扬州分公司九年级化学下册《酸碱盐》教学案新人教版课题酸碱盐学习目标与考点分析1.了解掌握酸碱盐的通性和特点
2.对酸碱盐化学性质的熟练记忆
3.记忆规律熟练应用到鉴别、推断、除杂当中
学情分析酸碱盐在整个中学化学中比较重要,必须对一些规律和性质通性能熟练记忆
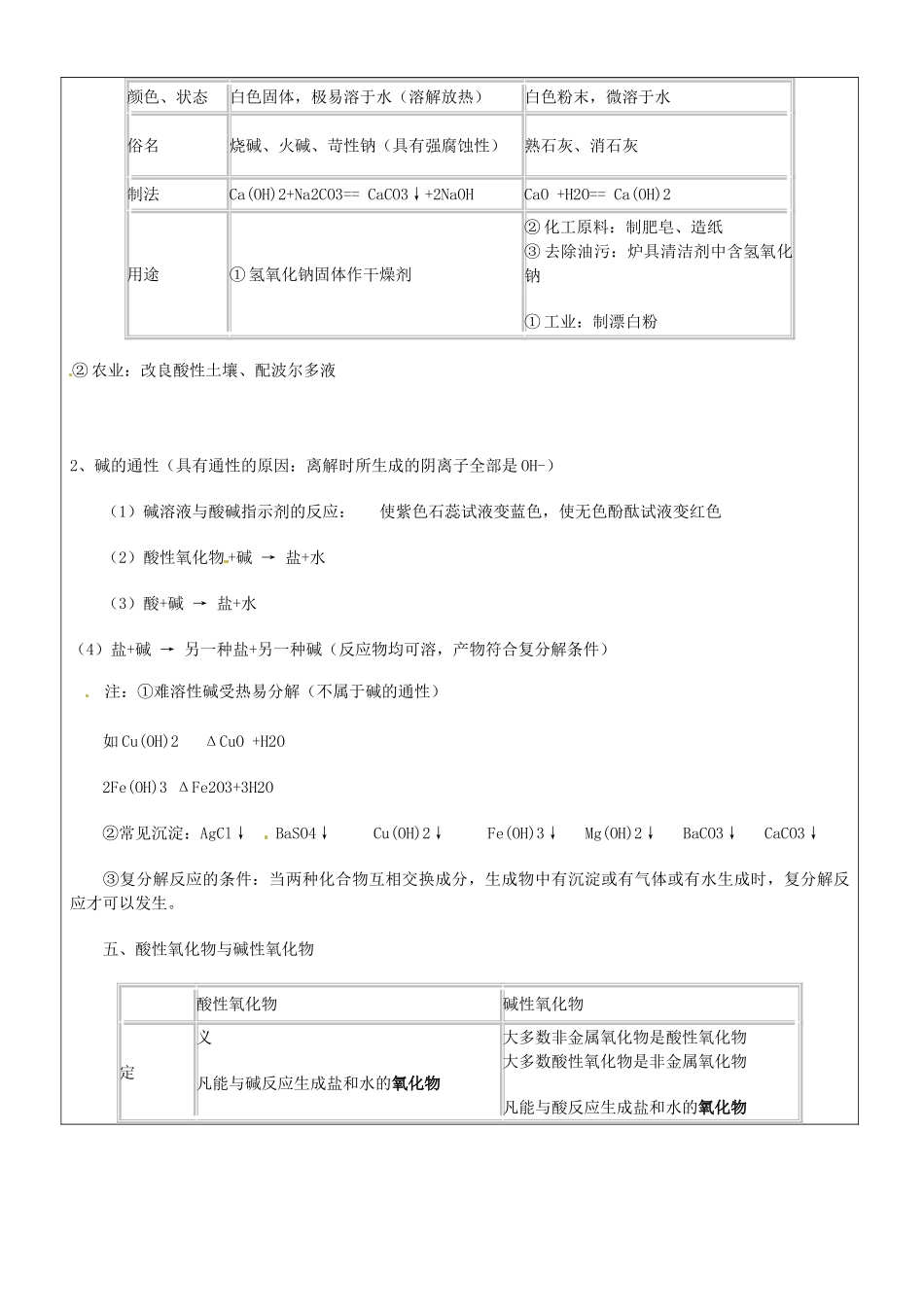
学习重难点如何将酸碱盐的基础知识,性质规律应用到实际解题当中教学方法教学提纲与过程第一部分:教学提纲一、酸、碱、盐的组成酸是由氢元素和酸根组成的化合物如:硫酸(H2SO4)、盐酸(HCl)、硝酸(HNO3)碱是由金属元素和氢氧根组成的化合物如:氢氧化钠、氢氧化钙、氨水(NH3·H2O)盐是由金属元素(或铵根)和酸根组成的化合物如:氯化钠、碳酸钠酸、碱、盐的水溶液可以导电(原因:溶于水时离解形成自由移动的阴、阳离子)二、酸1、浓盐酸、浓硫酸的物理性质、特性、用途浓盐酸浓硫酸颜色、状态“纯净”:无色液体工业用盐酸:黄色(含Fe3+)无色粘稠、油状液体气味有刺激性气味无特性挥发性(敞口置于空气中,瓶口有白雾)吸水性脱水性用途强氧化性腐蚀性①金属除锈②制造药物③人体中含有少量盐酸,助消化①金属除锈②浓硫酸作干燥剂2、酸的通性(具有通性的原因:酸离解时所生成的阳离子全部是H+)(1)与酸碱指示剂的反应:使紫色石蕊试液变红色,不能使无色酚酞试液变色(2)金属+酸→盐+氢气(3)碱性氧化物+酸→盐+水(4)碱+酸→盐+水(5)盐+酸→另一种盐+另一种酸(产物符合复分解条件)3、三种离子的检验三、碱1、氢氧化钠、氢氧化钙的物理性质、用途氢氧化钠氢氧化钙试剂Cl-AgNO3及HNO3SO42-①Ba(NO3)2及HNO3②HCl及BaCl2CO32-HCl及石灰水颜色、状态白色固体,极易溶于水(溶解放热)白色粉末,微溶于水俗名烧碱、火碱、苛性钠(具有强腐蚀性)熟石灰、消石灰制法Ca(OH)2+Na2CO3==