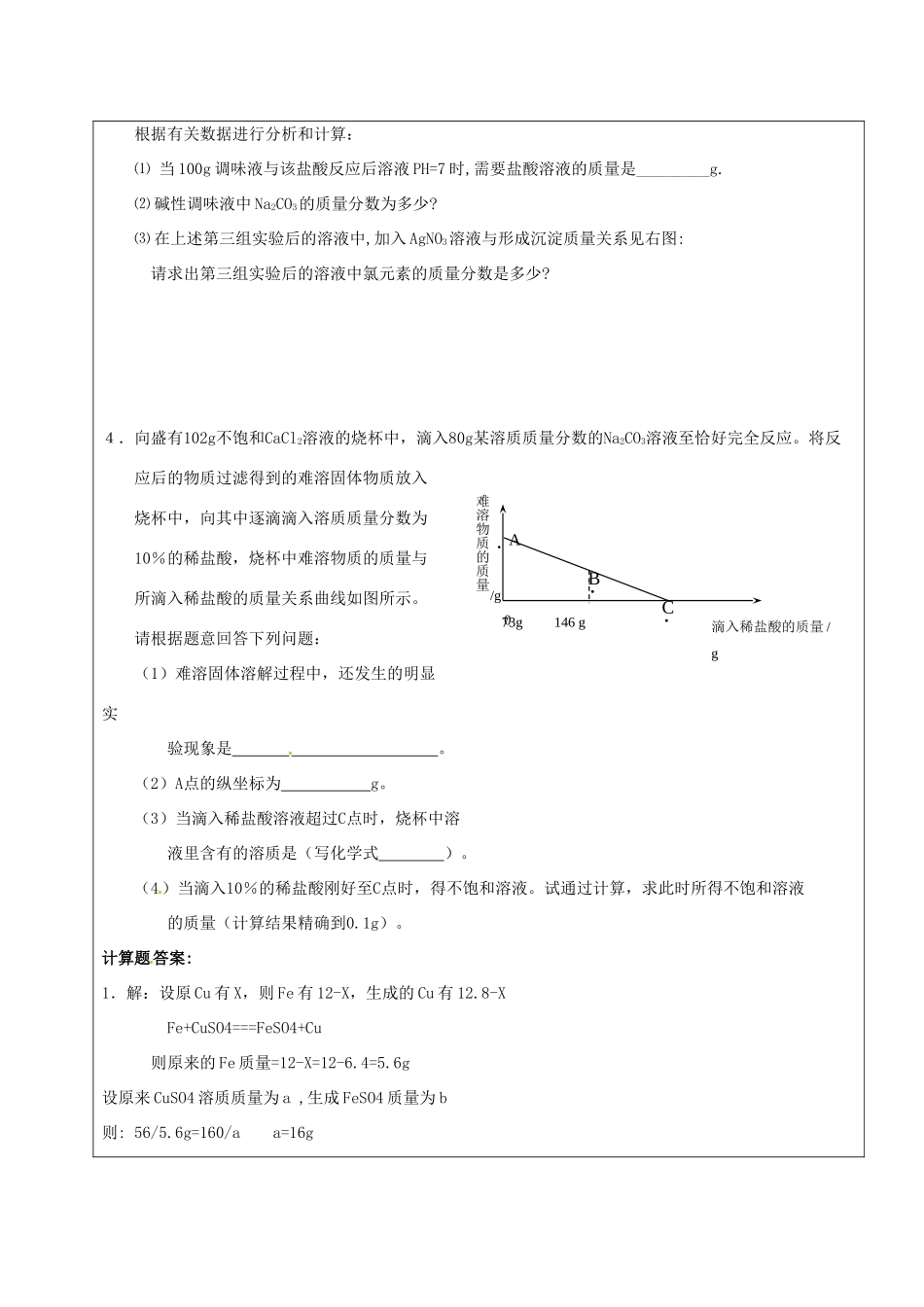
计算题教学目标知识目标牢固掌握化学式、化学方程式、溶解度、溶质的质量分数公式,并熟练计算能力目标培养学生熟练运用知识,提高应考能力情感目标振奋精神,激发斗志,增强自信教学重点熟练运用化学式、化学方程式、溶解度、溶质的质量分数公式,计算教学难点熟练运用化学式、化学方程式、溶解度、溶质的质量分数公式,计算主要教法归纳法,合作探究法,讲授法教学媒体多媒体教学过程1.小华同学取来Fe和Cu混合物12克,加入100克硫酸铜溶液中,恰好完全反应后,过滤,烘干固体称得12.8克,请你通过计算来判断溶液中溶质质量分数变大还是变小?2.将一定质量NaCl固体溶于103.4克水中得到不饱和溶液,再向所得溶液中小心加入300克AgNO3溶液。实验过程中,生成的AgCl质量与滴入的AgNO3溶液的质量关系如下图所示。⑴计算所加AgNO3溶液中溶质的质量分数。⑵计算B点溶液时溶液中NaNO3的质量分数。3.现有一种碱性调味液,是Na2CO3和NaCl组成的溶液。为了测定其中的溶质质量分数,设计了如下实验方案。取三份碱性调味液各100g,分别加入到50、100、150g某盐酸中,测得三组实验数据也下表。第一组第二组第三组盐酸溶液质量/g50100150生成气体质量/g2.24.45.5AgCl的质量/gAgNO3溶液的质量/g01003005.74AB沉淀的质量/gAgNO3溶液的质量/g057.4根据有关数据进行分析和计算:⑴当100g调味液与该盐酸反应后溶液PH=7时,需要盐酸溶液的质量是_________g.⑵碱性调味液中Na2CO3的质量分数为多少?⑶在上述第三组实验后的溶液中,加入AgNO3溶液与形成沉淀质量关系见右图:请求出第三组实验后的溶液中氯元素的质量分数是多少?4.向盛有102g不饱和CaCl2溶液的烧杯中,滴入80g某溶质质量分数的Na2CO3溶液至恰好完全反应。将反应后的物质过滤得到的难溶固体物质放入烧杯中,向其中逐滴滴入溶质质量分数为10%的稀盐酸,烧杯中难溶物质的质量与所滴入稀盐酸的质量关系曲线如图所示。请根据题意回答下列问题:(1)难溶固体溶解过程中,还发生的明显实验现象是。(2)A点的纵坐标为g。(3)当滴入稀盐酸溶液超过C点时,烧杯中溶液里含有的溶质是(写化学式)。(4)当滴入10%的稀盐酸刚好至C点时,得不饱和溶液。试通过计算,求此时所得不饱和溶液的质量(计算结果精确到0.1g)。计算题答案:1.解:设原Cu有X,则Fe有12-X,生成的Cu有12.8-XFe+CuSO4===FeSO4+Cu则原来的Fe质量=12-X=12-6.4=5.6g设原来CuSO4溶质质量为a,生成FeSO4质量为b则:56/5.6g=160/aa=16g滴入稀盐酸的质量/gAB难溶物质的质量/g73g146g0·C56/5.6g=152/bb=15.2g则原来溶液CuSO4%=16g/100g=16%反应后溶液中溶质质量分数FeSO4%=15.2/12g+100g-12.8g=15.3%15.3%<16%,所以反应后溶液中溶质质量分数变小.答:略(其它解答合理也可,如差量法等)学生总结解题步骤2.解:由图可知道当加入100gAgNO3溶液时,恰好完全反应.⑴设参加反应的AgNO3质量为X,NaCl+AgNO3=AgCl↓+NaNO3170143.5X5.74g170/X=143.5/5.74gX=6.8gAgNO3%=6.8g/100g×100%=6.8%⑵设NaCl的质量为Y,生成NaNO3的质量为ZNaCl+AgNO3=AgCl↓+NaNO358.5143.585Y5.74gZ58.5/Y=143.5/5.74gY=2.34g143.5/5.74g=85/ZZ=3.4g反应后溶液的质量为:2.34g+103.4g+300g-5.74g=400gNaNO3%=3.4g/400g×100%=0.85%答:略.(其它合理解答也可)3.解:⑴125g⑵通过二三组数据可知,第三组反应中酸过量,则碳酸钠被反应完。设参加反应的碳酸钠质量为X,Na2CO3+2HCl=2NaCl+H2O+CO2↑10644X5.5g106/X=44/5.5gX=13.25gNa2CO3%=13.25g/100g×100%=13.25%⑶第三组实验后的溶液中溶质有NaCl和HCl,但不管各多少质量,Cl-都会与Ag+形成沉淀,则AgCl中氯元素的质量等于第三组反应后混合液中氯元素的质量(元素质量守恒).因此,氯元素的质量==57.4g×35.5/143.5×100%=14.2g而第三组实验后的溶液质量=100g+150g-5.5g=244.5g所以,Cl%=14.2g/244.5g×100%=5.8%答:略(其它解法合理也可)4.(1)有气体生产(2)CaCO3+2HCl=CaCl2+H2O+CO2↑1007311144x156x10%yz=8.8X=20克所以A的纵坐标为20g.(3)CaCl2、HCl(4)y=22.2克质量分数=22.2/(156+20-8.8)x100%=12.5%小结:学完本节课你有哪些收获和疑问作业拓展:课后反思教学成败得失及改进设想: