课题一硫代硫酸钠与酸反应速率的影响因素【学考报告】知识条目加试要求①硫代硫酸钠和强酸反应的原理及实验现象②浓度、温度对硫代硫酸钠与酸反应速率的影响bc一、化学反应速率1
化学反应速率的概念化学反应速率是用来衡量化学反应进行快慢程度的物理量
化学反应速率的表示方法化学反应速率通常是用单位时间内反应物浓度的减小或生成物浓度的增加来表示,其数学表达式可表示为v=
式中Δc——某物质的浓度变化,常用单位为mol·L-1
Δt——时间变化,常用单位为s、min
v——某一物质的反应速率,常用单位是mol·L-1·s-1、mol·L-1·min-1等
影响化学反应速率的因素(1)反应物本身的性质是决定反应速率的内因
(2)外因:反应物浓度、温度、催化剂等
硫代硫酸钠与酸的反应向Na2S2O3溶液中加入稀硫酸,发生如下反应:Na2S2O3+H2SO4===Na2SO4+SO2↑+S↓+H2O,反应的离子方程式是S2O+2H+===SO2↑+S↓+H2O
由于反应生成不溶于水的S,使溶液出现浑浊现象
根据出现浑浊现象所需时间的长短,可以判断化学反应进行的快慢
反应进行得快,则先出现浑浊现象
二、课题方案设计1
实验操作要点为了比较实验中溶液出现浑浊的快慢,可以先在一张白纸上用黑色记号笔在合适的位置画上粗细、深浅一致的“十”字,衬在反应容器(锥形瓶)的底部
实验以Na2S2O3和H2SO4两溶液相混合时开始计时,到溶液出现的浑浊将锥形瓶底部的“十”字完全遮盖时结束
通过比较记录的反应所需时间,可以判断反应速率的大小
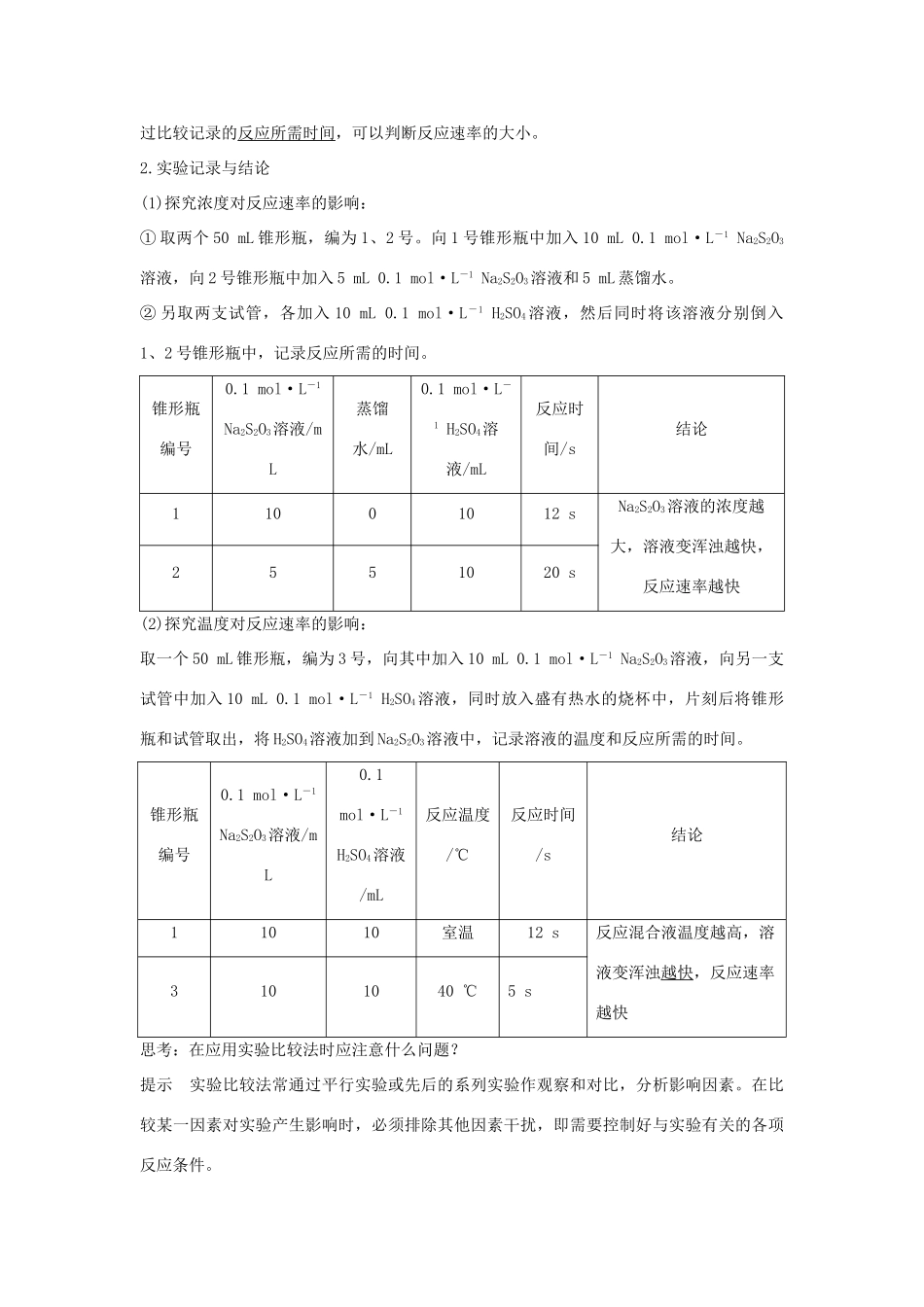
实验记录与结论(1)探究浓度对反应速率的影响:①取两个50mL锥形瓶,编为1、2号
向1号锥形瓶中加入10mL0
1mol·L-1Na2S2O3溶液,向2号锥形瓶中加入5mL0
1mol·L-1Na2S2O3溶液和5mL蒸馏水
②另取两支试管,各加入10mL0