第1课时认识有机化合物的一般性质和结构特点发展目标体系构建1
通过模型拼插等活动认识有机化合物分子的空间结构,能辨识常见有机化合物分子中的碳骨架
以甲烷、乙烯、乙炔为例认识碳原子成键的特点,知道常见有机化合物中碳原子的成键类型
一、认识有机化合物的一般性质1.概念有机化合物是指大多数含有碳元素的化合物
微点拨:CO、CO2、H2CO3及其盐属于无机物
2.性质(1)共性熔、沸点可燃性溶解性大多数熔、沸点低大多数可以燃烧大多难溶于水,易溶于有机溶剂微点拨:有机化合物的性质是指大多数有机物的性质,并不是绝对的
(2)差异性①挥发性:如乙醇、苯等易挥发,而甘油等难挥发
②溶解性:大多数难溶于水,但乙醇、乙酸等易溶于水
③热稳定性:大多数受热易分解,但酚醛树脂等具有较强热稳定性
④特征性质:许多有机化合物具有一定的特性,如乙醇能使紫色酸性KMnO4溶液褪色
二、有机化合物中碳原子的成键特点1.烃仅由碳和氢两种元素组成的有机化合物称为烃,也叫作碳氢化合物
CH4是组成最简单的烃
2.甲烷的组成与结构分子式结构式球棍模型填充模型CH4结构特点原子之间以单键结合,空间构型为正四面体形,碳原子位于正四面体的中心
有机物中碳原子的成键特点(1)每个碳原子能与其他原子形成4个共价键
(2)碳原子与碳原子之间可以形成单键()、双键()、三键(—C≡C—)
(3)碳原子之间彼此以共价键构成碳链或碳环
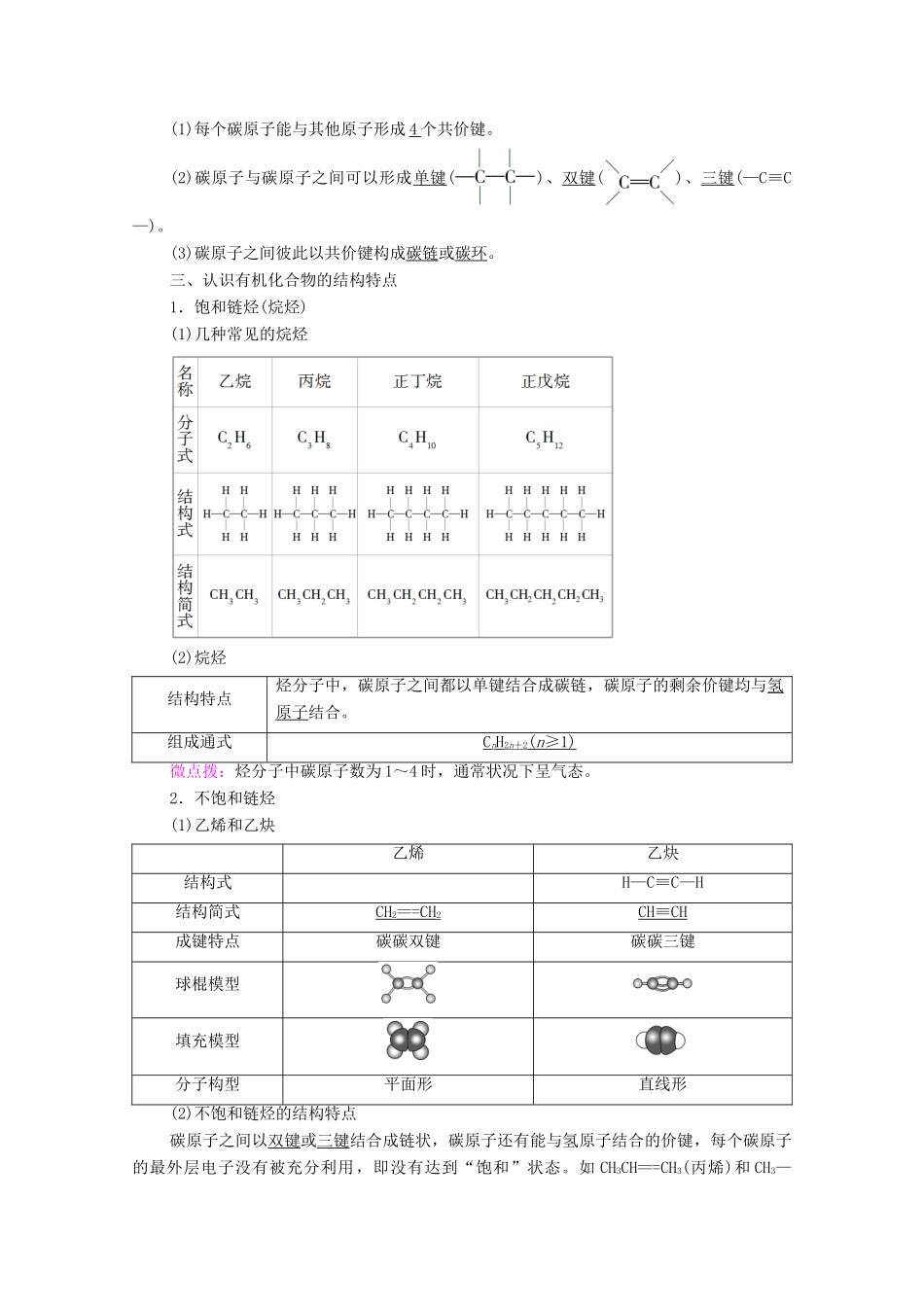
三、认识有机化合物的结构特点1.饱和链烃(烷烃)(1)几种常见的烷烃(2)烷烃结构特点烃分子中,碳原子之间都以单键结合成碳链,碳原子的剩余价键均与氢原子结合
组成通式CnH2n+2(n≥1)微点拨:烃分子中碳原子数为1~4时,通常状况下呈气态
2.不饱和链烃(1)乙烯和乙炔乙烯乙炔结构式H—C≡C—H结构简式CH2===CH2CH≡CH成键特点碳碳双键碳碳三键球棍模型填充模型分子构