第一章从实验学化学第二节化学计量在实验中的应用(第1课时)教学目标:1.使学生认识物质的量及其单位,能用于进行简单的化学计算
2.使学生知道引入物质的量这一物理量的重要性和必要性,知道阿伏加德罗常数的涵义
3.通过本部分的学习培养学生演绎推理、归纳推理的能力;调动学生参与知识形成的积极性和主动性
教学重点、难点重点:物质的量及其单位难点:物质的量及其单位教学环节教师活动学生活动导入新课物质之间的化学反应,是由肉眼不能看到的原子、分子或离子之间按一定数目关系进行的,同时又是以可称量的物质之间按一定的质量关系进行的
由此可见,在分子、原子等粒子与可称量的物质之间存在着某种联系,这是一种什么联系呢
怎样才能既科学又方便地知道一定量的物质中含有多少分子呢
这就是本节课所要解决的内容
(1)方程式2H2+O2=2H2O系数的意义是什么
(2)若生成一滴水(约0
05mL)大约含有1
7亿亿个水分子,需要氢气分子和氧气分子各多少个
(3)在实验室中生成36克水,你如何实现
是数分子个数吗
新知学习问题探究(1)怎样测量课本中一张纸的厚度
又怎样知道一个水分子的质量呢
归纳整理显然,可用确定一个集体的办法,确定一个水分子的集体,这一定数目水分子(粒子)的集体,就把水(可称量物)与水分子(粒子)联系起来了
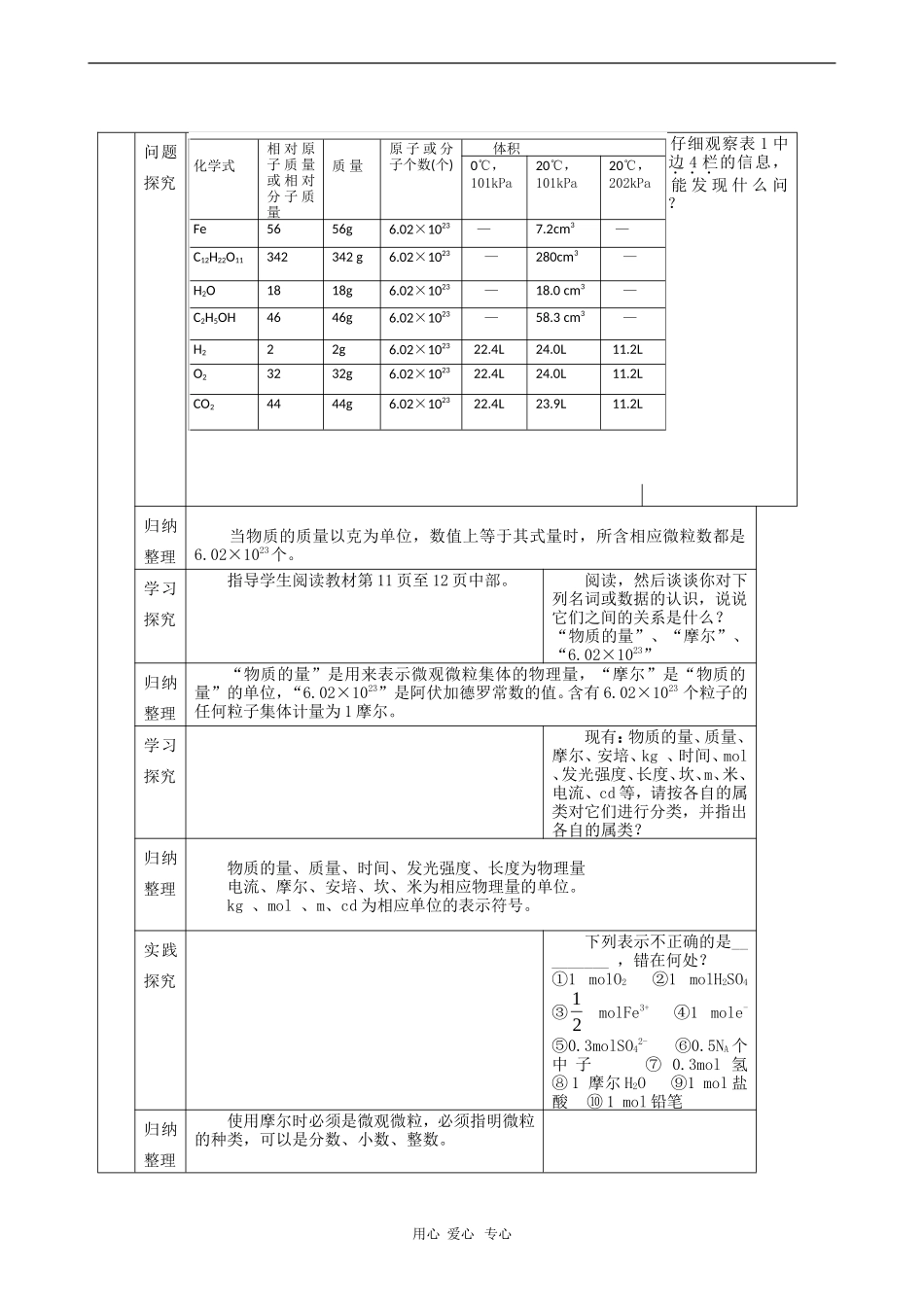
用心爱心专心问题探究仔细观察表1中左边4栏的信息,你能发现什么问题
归纳整理当物质的质量以克为单位,数值上等于其式量时,所含相应微粒数都是6
02×1023个
学习探究指导学生阅读教材第11页至12页中部
阅读,然后谈谈你对下列名词或数据的认识,说说它们之间的关系是什么
“物质的量”、“摩尔”、“6
02×1023”归纳整理“物质的量”是用来表示微观微粒集体的物理量,“摩尔”是“物质的量”的单位,“6
02×1023”是阿伏加德罗常数的值
02×1023个粒子的任何粒子集体计量为