第1课时硫与二氧化硫[学习目标]1
能从物质类别、元素化合价角度依据复分解反应规律和氧化还原反应原理,预测S、SO2的性质及其转化,设计实验进行初步验证,并能用化学方程式、离子方程式正确表示S、SO2的主要化学性质
能说明S、SO2的应用对社会发展的价值和对环境的影响
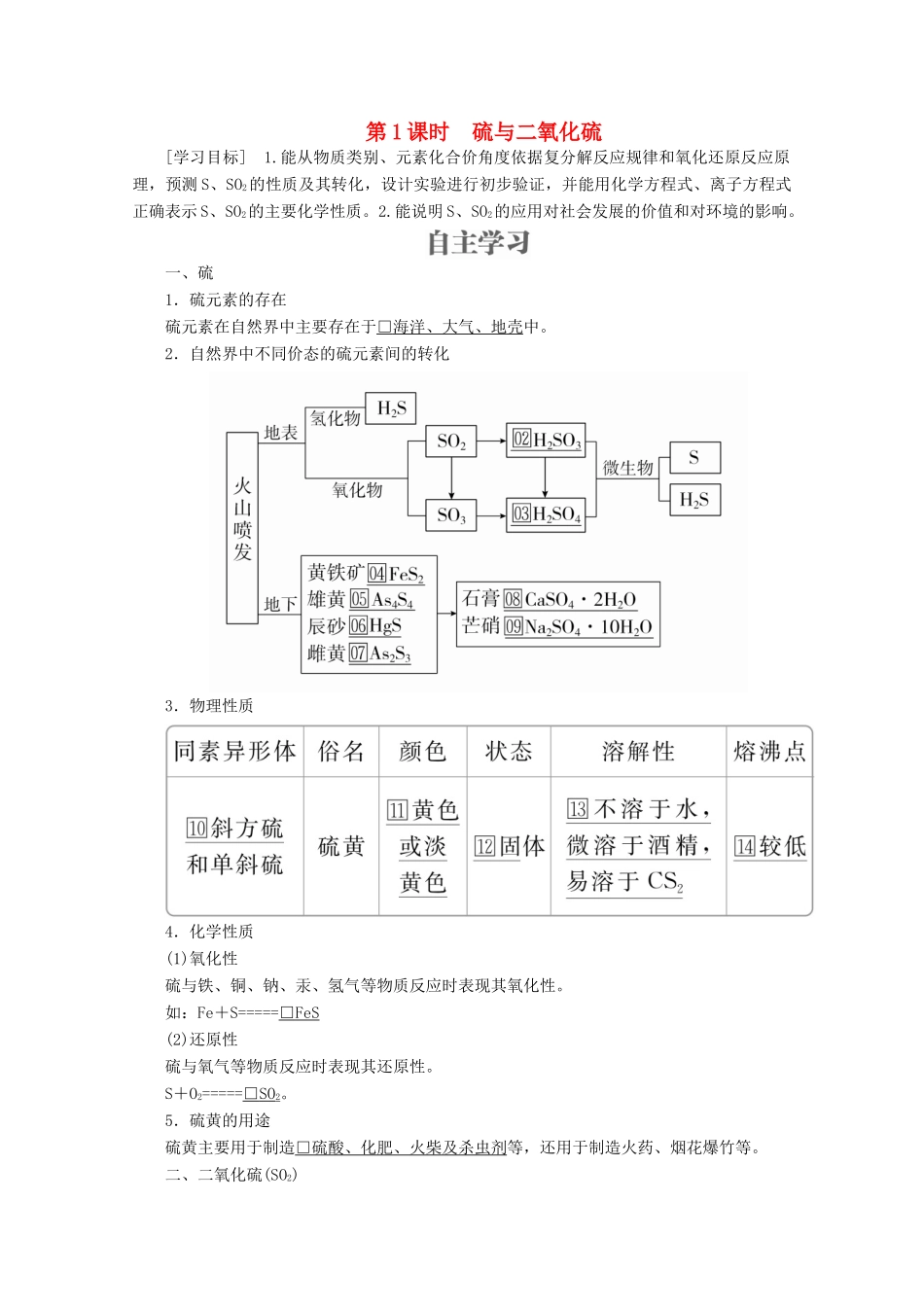
一、硫1.硫元素的存在硫元素在自然界中主要存在于□海洋、大气、地壳中
2.自然界中不同价态的硫元素间的转化3.物理性质4.化学性质(1)氧化性硫与铁、铜、钠、汞、氢气等物质反应时表现其氧化性
如:Fe+S=====□FeS(2)还原性硫与氧气等物质反应时表现其还原性
S+O2=====□SO2
5.硫黄的用途硫黄主要用于制造□硫酸、化肥、火柴及杀虫剂等,还用于制造火药、烟花爆竹等
二、二氧化硫(SO2)1.物理性质二氧化硫为□无色、□有刺激性气味的□有毒□气体,密度比空气的大,易液化(沸点为-10℃),□易溶于水
在常温、常压下,1体积水大约能溶解40体积的二氧化硫
2.化学性质SO2属于□酸性氧化物,具有酸性氧化物的通性;SO2中硫元素的化合价为+4,SO2既有□氧化性又有□还原性,但以□还原性为主
(1)具有酸性氧化物的通性(2)既有还原性,又有氧化性还原性:2SO2+O2((((2SO3SO2+X2+2H2O===□H2SO4+2HX(X=Cl、Br、I)5SO2+2MnO+2H2O===5SO+2Mn2++4H+SO2+2Fe3++2H2O===+2Fe2++□4H+氧化性:SO2的氧化性较弱,只有在存在较强还原剂(如H2S)的情况下,才会表现出氧化性
SO2+2H2S===□3S↓+2H2O(3)漂白性SO2具有漂白性,能使某些有色物质退色
将SO2通入品红溶液中,品红溶液退色,加热后溶液又恢复为原来的颜色,利用这一原理可以检验SO2的存在
一、硫单质的性质及用途[交流研讨]自然界中存在的含硫的