第2课时化学电源发展目标体系构建1
知道化学电源的分类方法
熟悉几种常见化学电源的组成和工作原理
了解化学电源广泛的应用及废旧电池对环境的危害,设想其处理方法
一、化学电源1.概念化学电源是将化学能变成电能的装置
2.分类3.判断电池优劣的主要标准(1)比能量:即单位质量或单位体积所能输出电能的多少,单位(W·h)/kg或(W·h)/L
(2)比功率:即单位质量或单位体积所能输出功率的多少,单位W/kg或W/L
(3)电池的可储存时间的长短
二、一次电池1.一次电池随着使用,一次电池中能发生氧化还原反应的物质被消耗,当这些物质消耗到一定程度时,电池就不能继续使用了
一次电池中电解质溶液制成胶状,不流动,也叫做干电池
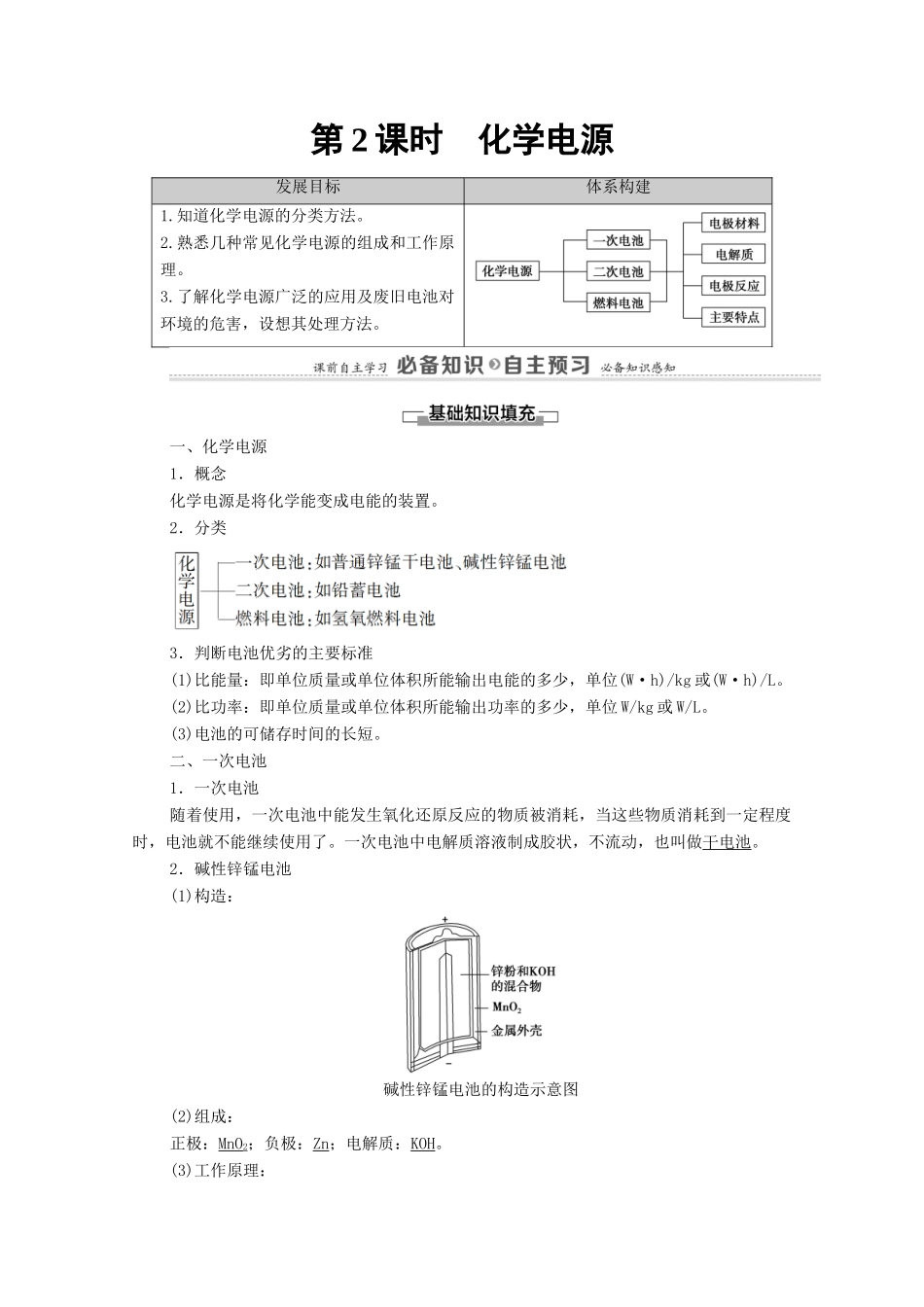
2.碱性锌锰电池(1)构造:碱性锌锰电池的构造示意图(2)组成:正极:MnO2;负极:Zn;电解质:KOH
(3)工作原理:负极:Zn+2OH--2e-===Zn(OH)2;正极:2MnO2+2H2O+2e-===2MnO(OH)+2OH-;总反应:Zn+2MnO2+2H2O===2MnO(OH)+Zn(OH)2
碱性锌锰电池比普通锌锰电池有哪些优良性能
[提示]比能量和可储存时间均有所提高,适用于大电流和连续放电
三、二次电池铅蓄电池是常见的二次电池,其放电反应和充电反应表示如下:Pb(s)+PbO2(s)+2H2SO4(aq)2PbSO4(s)+2H2O(l)(1)负极是Pb,正极是PbO2,电解质溶液是硫酸溶液
(2)放电反应原理①负极反应式是Pb(s)+SO(aq)-2e-===PbSO4(s);②正极反应式是PbO2(s)+4H+(aq)+SO(aq)+2e-===PbSO4(s)+2H2O(l);③放电过程中,负极质量的变化是增大,电解质溶液pH的变化是增大
(3)充电反应原理①阴极(发生还原反应)反应式是PbSO4(s)+2e-===Pb(