第一节共价键发展目标体系构建1
能从微观角度分析形成共价键的粒子、类型,能辨识物质中含有的共价键的类型及成键方式,了解键能、键长及键角对物质性质的影响
理解共价键中σ键和π键的区别,建立判断σ键和π键的思维模型,熟练判断分子中σ键和π键的存在及个数
一、共价键1.共价键的概念和特征原子间通过共用电子对所形成的相互作用
微点拨:共价键的方向性决定了分子的立体构型,并不是所有共价键都具有方向性,如两个s电子形成共价键时就没有方向性
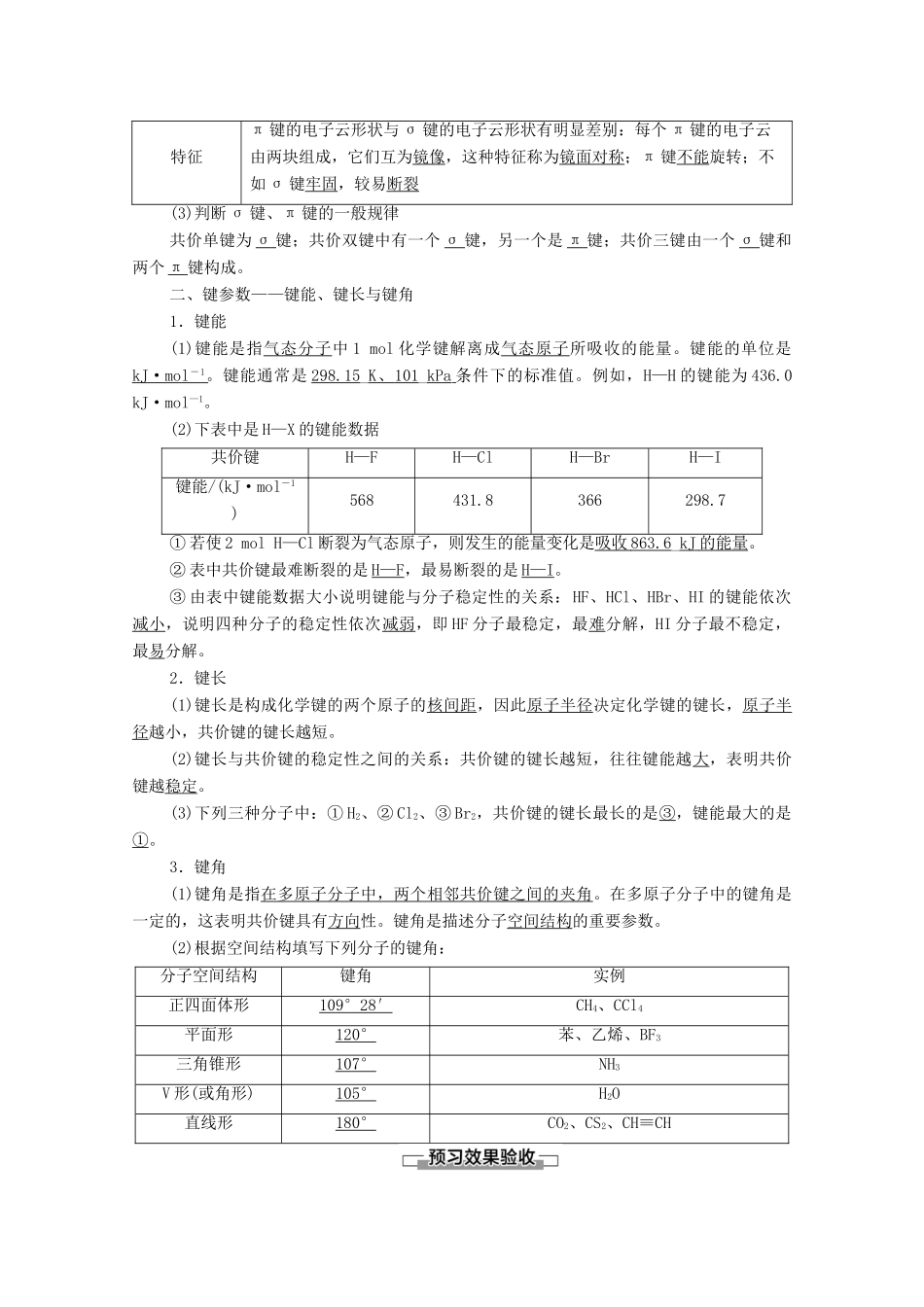
2.共价键的类型(按成键原子的原子轨道重叠方式分类)(1)σ键形成由成键原子的s轨道或p轨道重叠形成类型s-s型s-p型p-p型特征以形成化学键的两原子核的连线为轴做旋转操作,共价键的电子云的图形不变,这种特征称为轴对称(2)π键形成由两个原子的p轨道“肩并肩”重叠形成p-pπ键特征π键的电子云形状与σ键的电子云形状有明显差别:每个π键的电子云由两块组成,它们互为镜像,这种特征称为镜面对称;π键不能旋转;不如σ键牢固,较易断裂(3)判断σ键、π键的一般规律共价单键为σ键;共价双键中有一个σ键,另一个是π键;共价三键由一个σ键和两个π键构成
二、键参数——键能、键长与键角1.键能(1)键能是指气态分子中1mol化学键解离成气态原子所吸收的能量
键能的单位是kJ·mol-1
键能通常是298
15_K、101_kPa条件下的标准值
例如,H—H的键能为436
0kJ·mol—1
(2)下表中是H—X的键能数据共价键H—FH—ClH—BrH—I键能/(kJ·mol-1)568431
8366298
7①若使2molH—Cl断裂为气态原子,则发生的能量变化是吸收863
6_kJ的能量
②表中共价键最难断裂的是H—F,最易断裂的是H—I
③由表中键能数据大小说明键能与分子稳定性的关系:HF、HCl、HBr、HI的键能依次减小,说明四种分子的稳定性依次减弱,