第2课时价层电子对互斥理论等电子原理[核心素养发展目标]1
了解价层电子对互斥理论,通过对价层电子对互斥模型的探究,建立判断分子空间构型的思维模型
了解等电子体的概念及判断方法,能用等电子原理解释物质的结构和某些性质
一、价层电子对互斥模型1.价层电子对互斥模型的基本内容分子中的价电子对(包括成键电子对和孤电子对)由于相互排斥作用,而趋向于尽可能彼此远离以减小斥力,分子尽可能采取对称的空间构型
(1)当中心原子的价电子全部参与成键时,为使价电子斥力最小,就要求尽可能采取对称结构
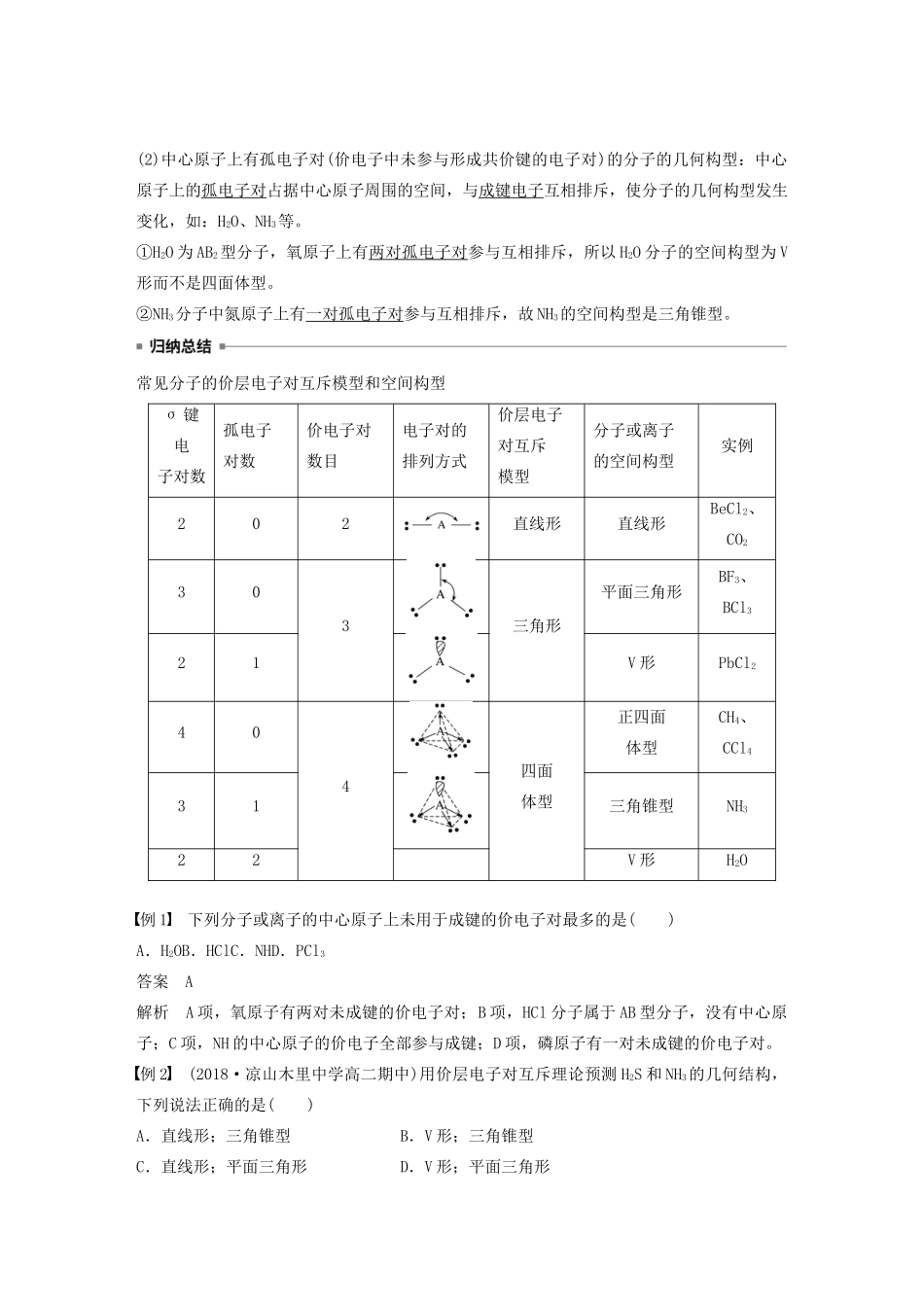
(2)当中心原子的价电子部分参与成键时,未参与成键的孤电子对与成键电子对之间及孤电子对之间、成键电子对之间的斥力不同,从而影响分子的空间构型
(3)电子对之间的夹角越大,相互之间的斥力越小
2.价电子对的计算(1)ABm型分子中心原子价层电子对数目的计算方法ABm型分子(A是中心原子,B是配位原子)中价层电子对数n的计算:n=(2)在计算中心原子的价层电子对数时应注意如下规定①作为配位原子,卤素原子和H原子提供1个电子,氧族元素的原子不提供电子;②作为中心原子,卤素原子按提供7个电子计算,氧族元素的原子按提供6个电子计算;③对于复杂离子,在计算价层电子对数时,还应加上负离子的电荷数或减去正离子的电荷数
如PO中P原子价层电子数应加上3,而NH中N原子的价层电子数应减去1;④计算电子对数时,若剩余1个电子,即出现奇数电子,也把这个单电子当作1对电子处理;⑤双键、叁键等多重键作为1对电子看待
3.价层电子对互斥模型与分子的几何构型(1)中心原子中的价电子全部参与形成共价键的分子的几何构型如下表所示(由中心原子周围的原子数m来预测):ABm几何构型示例m=2直线形CO2、BeCl2m=3平面三角形CH2O、BF3m=4正四面体CH4、CCl4(2)中心原子上有孤电子对(价电子中未参与形成共价键的电子对