高考化学专题“电解质溶液”分析及教学建议●高考趋势展望电解质溶液是高中化学重要的基础理论之一,从近几年的高考试题可以看出,涉及电解质溶液的考点多,重现率高
其主要热点是:1
外界条件对电离平衡的影响、强弱电解质的比较;2
酸、碱混合后溶液的酸碱性的判断及pH的计算,已知混合后溶液的pH推断混合前的各种可能;3
盐对水的电离程度的影响、盐溶液蒸干灼烧后产物的判断、离子浓度大小的比较等
由于相同条件下强弱电解质的导电能力有着本质区别,因此,强弱电解质可通过同条件下电流的大小来确定,这一导电实验是理化学科的结合点,同时弱电解质的有关量也会因电离程度发生变化而难以确定其大小,此时常常需用数学思维方法(如极值法)进行处理
溶液的pH计算题设条件可千变万化,正向与逆向思维、数字与字母交替出现,与生物酸碱平衡相结合或运用数学工具进行推理等试题在“3+X”综合测试中出现的可能性极大,展望今后会以填空或选择的形式出现,题目难度适中,推理性会有所增强
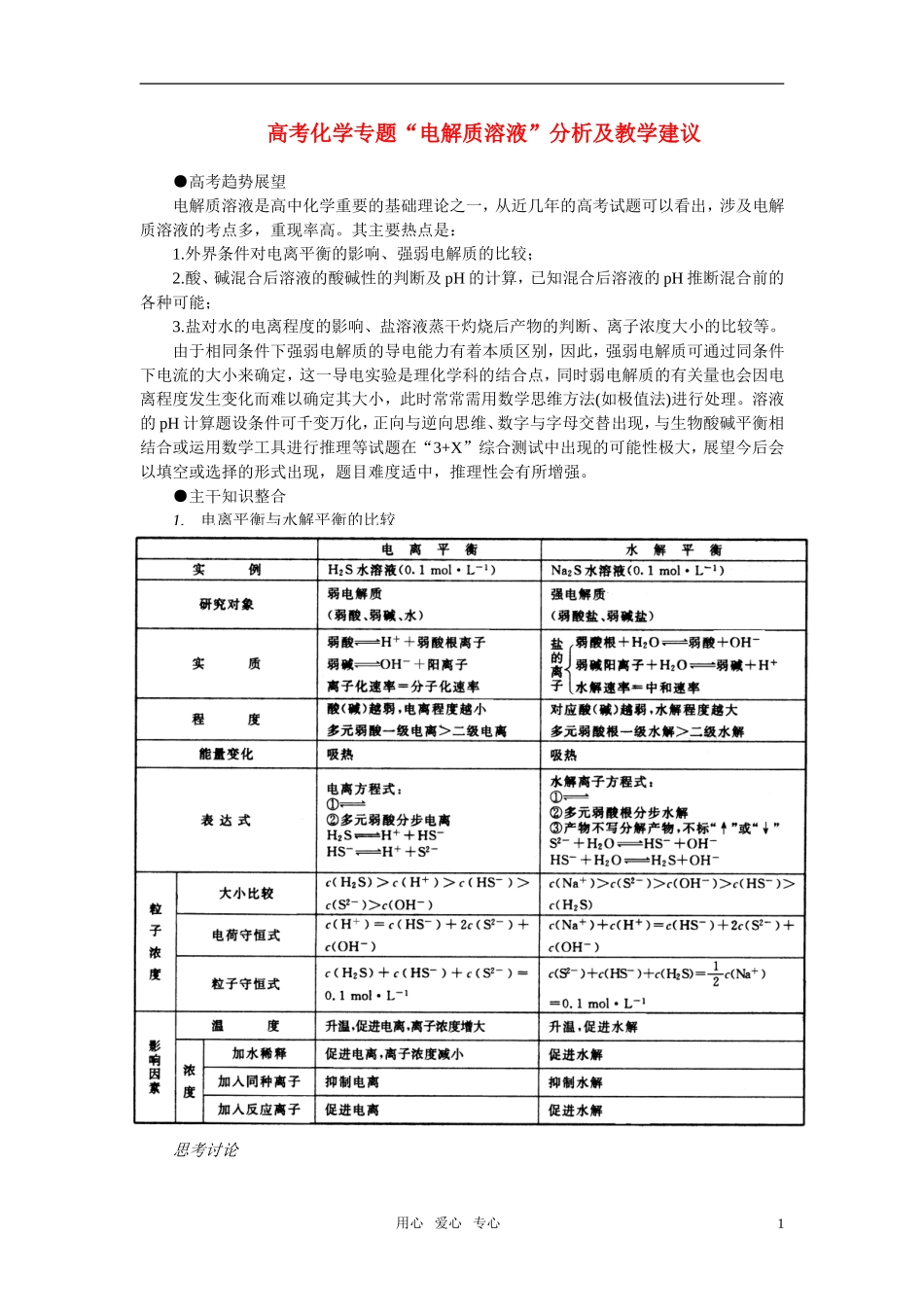
●主干知识整合1
电离平衡与水解平衡的比较思考讨论用心爱心专心1已知在相同条件下NH3·H2O与CH3COOH电离程度几乎相等,CH3COOH的酸性比H2CO3强,那么NH4HCO3溶液显酸性、碱性还是中性
因为H2CO3比醋酸弱,HCO的水解能力比CH3COO-强,而CH3COO-的水解能力与相当,故HCO水解能力比强,因此,该溶液应显碱性
溶液酸碱性判定规律(1)pH相同的酸(或碱),酸(或碱)性越弱,其物质的量浓度越大
(2)pH相同的强酸和弱酸溶液,加水稀释相同的倍数,则强酸溶液pH变化大;碱也如此
(3)酸与碱的pH之和为14,等体积混合①若为强酸与强碱则pH=7;②若为强酸与弱碱则pH>7;③若为弱酸与强碱则pH<7
(4)等体积强酸和强碱混合①若二者pH之和为14,则溶液呈中性,pH=7;②若二者pH之和大于14,则