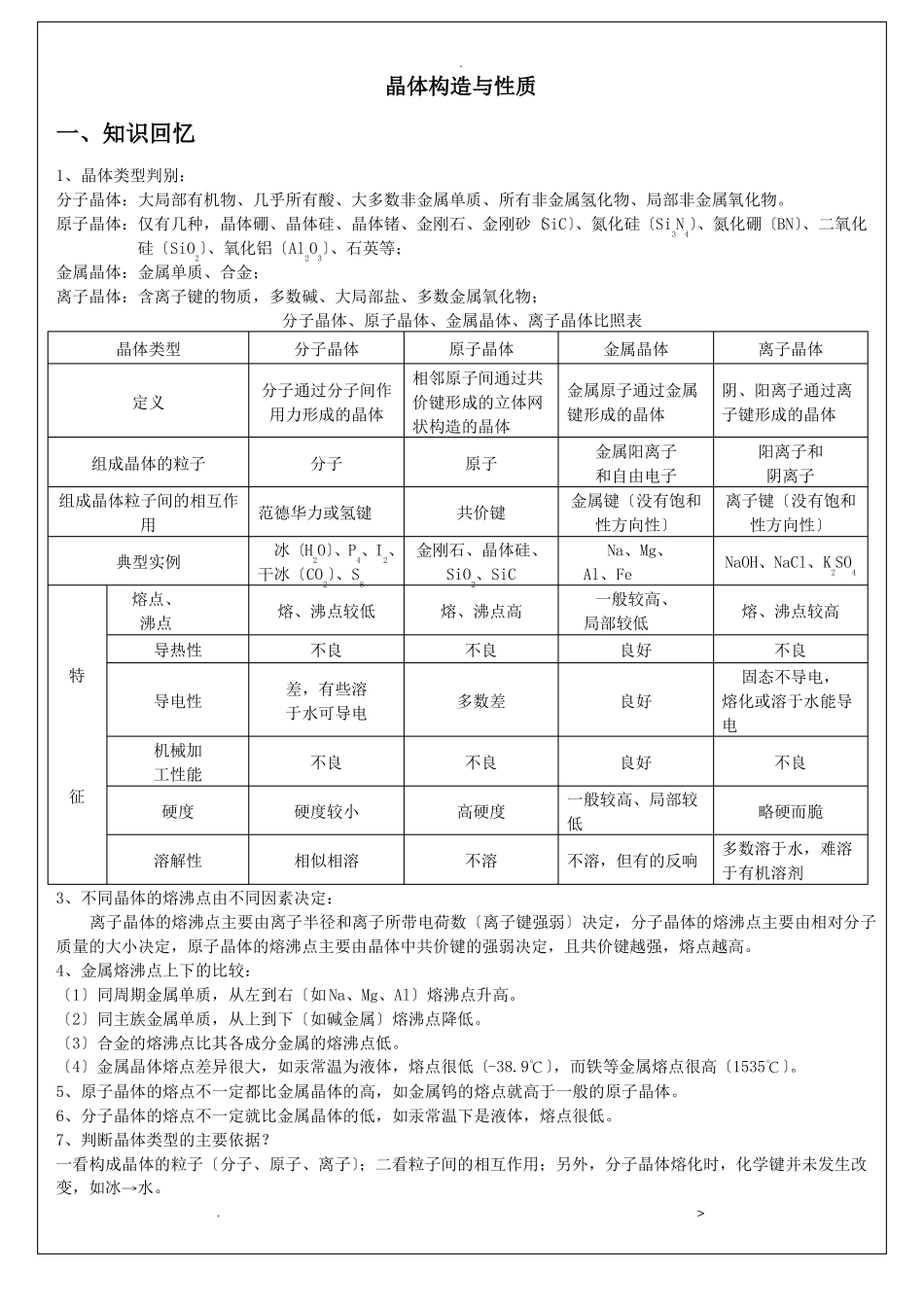
晶体构造与性质一、知识回忆1、晶体类型判别:分子晶体:大局部有机物、几乎所有酸、大多数非金属单质、所有非金属氢化物、局部非金属氧化物
原子晶体:仅有几种,晶体硼、晶体硅、晶体锗、金刚石、金刚砂〔SiC〕、氮化硅〔Si3N4〕、氮化硼〔BN〕、二氧化硅〔SiO2〕、氧化铝〔Al2O3〕、石英等;金属晶体:金属单质、合金;离子晶体:含离子键的物质,多数碱、大局部盐、多数金属氧化物;分子晶体、原子晶体、金属晶体、离子晶体比照表晶体类型定义分子晶体分子通过分子间作用力形成的晶体分子范德华力或氢键原子晶体相邻原子间通过共价键形成的立体网状构造的晶体原子共价键金属晶体金属原子通过金属键形成的晶体金属阳离子和自由电子金属键〔没有饱和性方向性〕Na、Mg、Al、Fe一般较高、局部较低良好良好离子晶体阴、阳离子通过离子键形成的晶体阳离子和阴离子离子键〔没有饱和性方向性〕NaOH、NaCl、K2SO4熔、沸点较高不良固态不导电,熔化或溶于水能导电不良略硬而脆多数溶于水,难溶于有机溶剂组成晶体的粒子组成晶体粒子间的相互作用典型实例熔点、沸点导热性特征导电性机械加工性能硬度溶解性冰〔H2O〕、P4、I2、金刚石、晶体硅、干冰〔CO2〕、S8SiO2、SiC熔、沸点较低不良差,有些溶于水可导电不良硬度较小相似相溶熔、沸点高不良多数差不良高硬度不溶良好一般较高、局部较低不溶,但有的反响3、不同晶体的熔沸点由不同因素决定:离子晶体的熔沸点主要由离子半径和离子所带电荷数〔离子键强弱〕决定,分子晶体的熔沸点主要由相对分子质量的大小决定,原子晶体的熔沸点主要由晶体中共价键的强弱决定,且共价键越强,熔点越高
4、金属熔沸点上下的比较:〔1〕同周期金属单质,从左到右〔如Na、Mg、Al〕熔沸点升高
〔2〕同主族金属单质,从上到下〔如碱金属〕熔沸点降低
〔3〕合金的熔沸点比其各成分金属的熔沸点低
〔4〕金属晶体熔