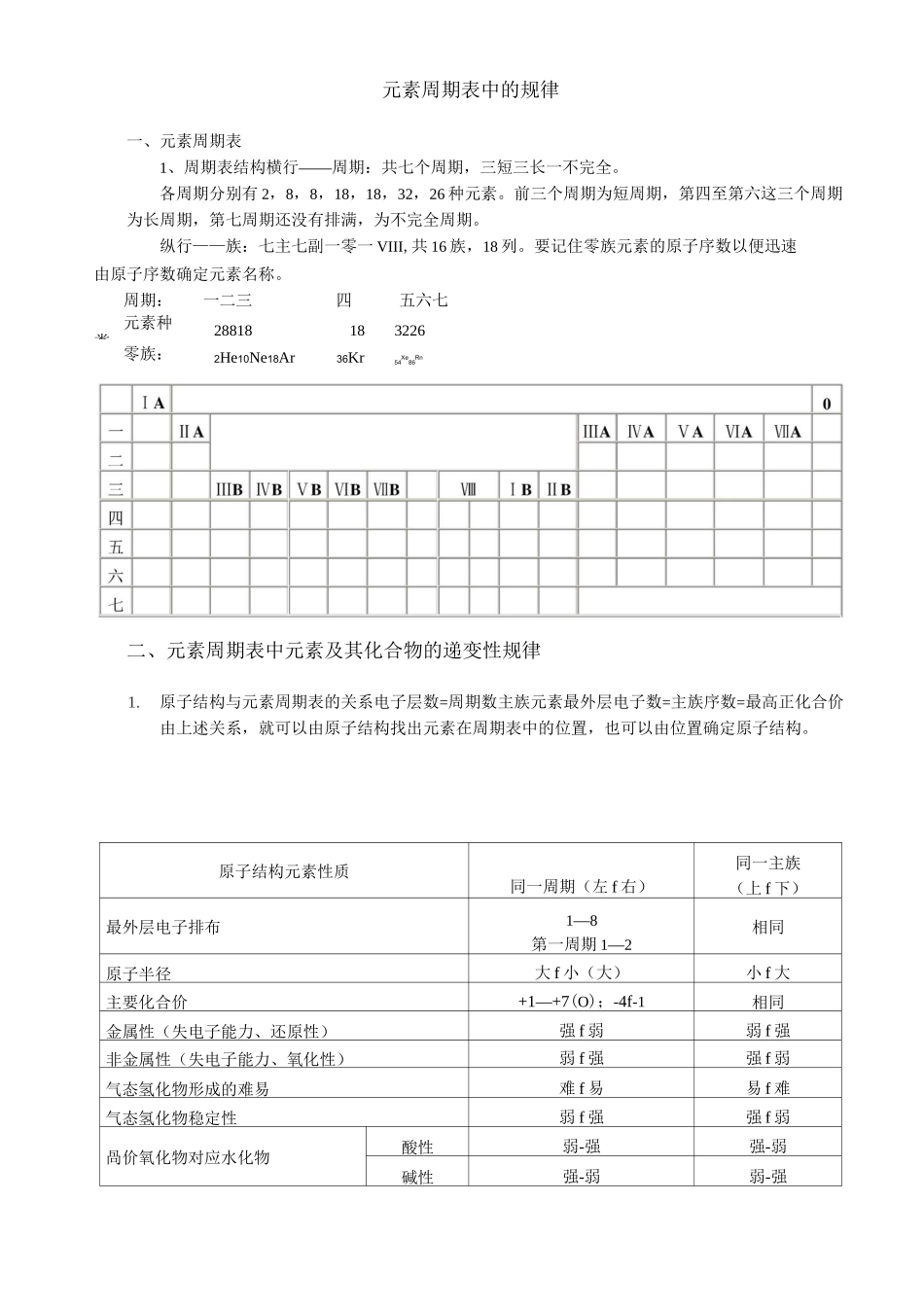
元素周期表中的规律一、元素周期表1、周期表结构横行——周期:共七个周期,三短三长一不完全
各周期分别有2,8,8,18,18,32,26种元素
前三个周期为短周期,第四至第六这三个周期为长周期,第七周期还没有排满,为不完全周期
纵行——族:七主七副一零一VIII,共16族,18列
要记住零族元素的原子序数以便迅速由原子序数确定元素名称
周期:一二三四五六七元素种类:28818183226零族:2He10Ne18Ar36Kr54Xe86Rn二、元素周期表中元素及其化合物的递变性规律1
原子结构与元素周期表的关系电子层数=周期数主族元素最外层电子数=主族序数=最高正化合价由上述关系,就可以由原子结构找出元素在周期表中的位置,也可以由位置确定原子结构
原子结构元素性质同一周期(左f右)同一主族(上f下)最外层电子排布1—8第一周期1—2相同原子半径大f小(大)小f大主要化合价+1—+7(O);-4f-1相同金属性(失电子能力、还原性)强f弱弱f强非金属性(失电子能力、氧化性)弱f强强f弱气态氢化物形成的难易难f易易f难气态氢化物稳定性弱f强强f弱咼价氧化物对应水化物酸性弱-强强-弱碱性强-弱弱-强非金厲性■笠隅性5由此可见,金属性最强的元素在周期表的左下角即Cs(Fr具有放射性,不考虑),非金属性最强的元素在右上角即F
对角线附近的元素不是典型的金属元素或典型的非金属元素
3、元素周期表中之最原子半径最小的原子:H原子质量最轻的元素:H元素;非金属性最强的元素:F金属性最强的元素:Cs(不考虑Fr)最高价氧化物对应水化物酸性最强的酸:HCIO4最高价氧化物对应水化物碱性最强的碱:CsOH形成化合物最多的元素:C元素所含元素种类最多的族:IIIB地壳中含量最高的元素:O元素,其次是Si元素地壳中含量最高的金属元素:Al元素,其次是Fe元素含H质量分数最高的气态氢化物:CH4与水反应