课题3溶液的浓度人教新课标版(2012教材)九下第九单元温故而知新1、饱和溶液在一定温度下、一定量的溶剂中,溶质不能继续溶解的溶液
2、饱和溶液和不饱和溶液之间的相互转化方法不饱和溶液饱和溶液蒸发溶剂增加溶质降低温度增加溶剂升高温度3、固体溶解度在一定温度下,某固态物质在100克溶剂里达到饱和状态时所溶解的质量,叫做这种物质在这种溶剂里的溶解度
4、气体溶解度指该气体的压强为101KPa和一定温度时,在1体积水里溶解达到饱和状态时的气体体积
第一课时[实验9-7]试管编号溶液颜色溶剂质量溶质质量溶液质量(1)浅200
1(2)较浅200
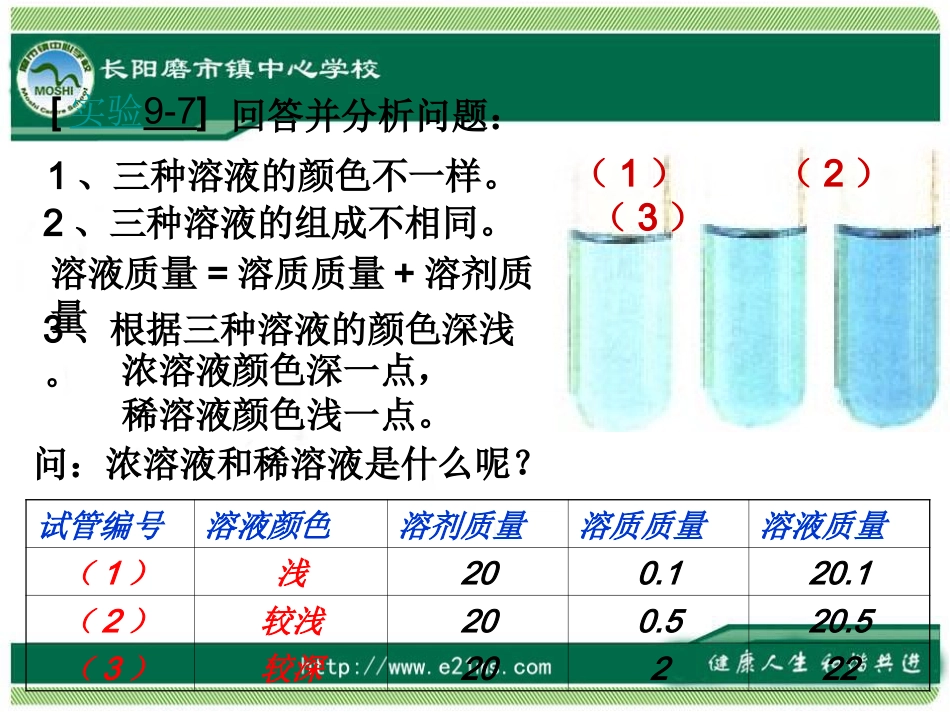
5(3)较深20222(1)(2)(3)回答并分析问题:1、三种溶液的颜色不一样
2、三种溶液的组成不相同
3、根据三种溶液的颜色深浅
浓溶液颜色深一点,稀溶液颜色浅一点
问:浓溶液和稀溶液是什么呢
溶液质量=溶质质量+溶剂质量“浓溶液”和“稀溶液”是由溶质和溶剂共同决定的,表示溶液里相对溶质的含量多少
浓溶液稀溶液饱和溶液不饱和溶液一、溶液的浓度1、定义:溶质的质量分数溶质的体积分数溶质的质量分数=×100%溶质质量溶液质量二、溶质的质量分数3、公式变形:一定量的溶液里所含溶质的量2、表示方法:1、定义:溶质的质量与溶液的质量之比2、公式:溶质质量=溶液质量×溶质的质量分数溶液的质量=溶质的质量+溶剂的质量=溶液的体积×溶液的密度练一练:请把实验9-7中溶液的溶质质量分数填在表格中
试管编号溶液颜色溶剂质量溶质质量溶液质量溶质的质量分数(1)浅20g0
1g(2)较浅20g0
5g(3)较深20g2g22g0
1%1、已知溶质和溶剂的量,求溶质的质量分数;三、关于溶质的质量分数计算类型:[实验9-8]:按下表所定的量配制氯化钠溶液并计算
溶质质量/g溶剂(水)质量/g现象溶液中溶质的质量