非金属实验题专项练习1
两个化学兴趣小组进行了以下探究活动:第一组:为研究铁质材料与热浓硫酸的反应(l)称取铁钉(碳素钢)12
0g放入30
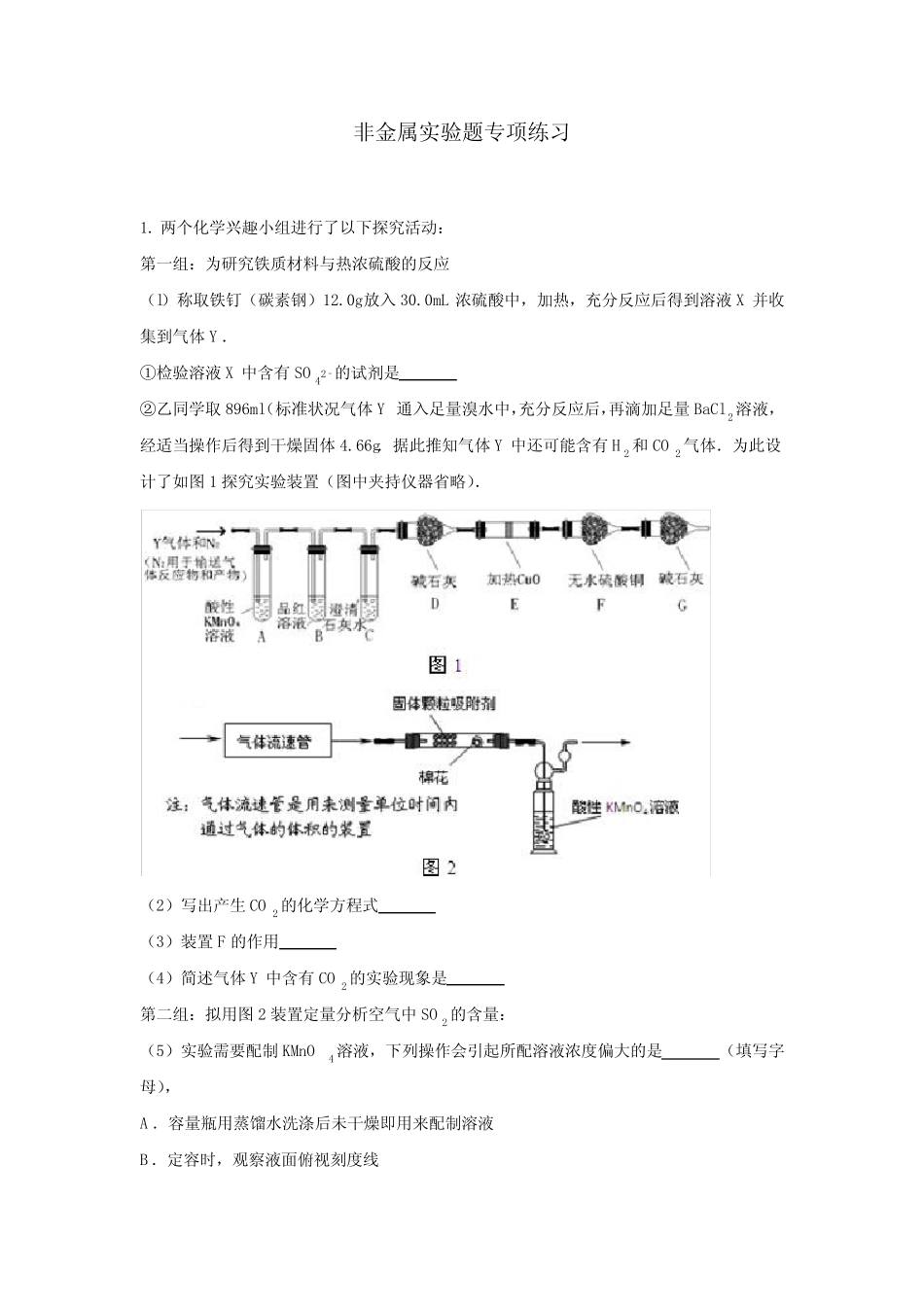
0mL浓硫酸中,加热,充分反应后得到溶液X并收集到气体Y.①检验溶液X中含有SO42﹣的试剂是②乙同学取896ml(标准状况气体Y通入足量溴水中,充分反应后,再滴加足量BaCl2溶液,经适当操作后得到干燥固体4
66g.据此推知气体Y中还可能含有H2和CO2气体.为此设计了如图1探究实验装置(图中夹持仪器省略).(2)写出产生CO2的化学方程式(3)装置F的作用(4)简述气体Y中含有CO2的实验现象是第二组:拟用图2装置定量分析空气中SO2的含量:(5)实验需要配制KMnO4溶液,下列操作会引起所配溶液浓度偏大的是(填写字母),A.容量瓶用蒸馏水洗涤后未干燥即用来配制溶液B.定容时,观察液面俯视刻度线C.摇匀后,液面低于刻度线,没有再加蒸馏水D.用蒸馏水洗涤烧杯和玻璃棒.并将洗涤液转移入容量瓶中(6)该实验中已经知道的数据有气体流速aL/min、酸性KMnO4溶液的体积bL,其浓度为cmol/L.若从气体通入到紫色恰好褪去,用时5分钟.则此次取样处的空气中二氧化硫含量为g/L.答案:(1)①检验SO42﹣:先加入过量稀盐酸,以除去SO32﹣、CO32﹣等离子的影响,同时,当加入稀盐酸时没有沉淀,可排除Cl﹣的影响.故答案为:HCl、BaCl2;(2)答案:C+2H2SO4(浓)CO2↑+2SO2↑+2H2O;(3)答案:检验是否有水蒸气产生;(4)确认气体Y中含有CO2,应完全排除二氧化硫的干扰,当B中品红溶液不褪色,C中石灰水变浑浊,可说明含有CO2,答案为:B中品红不褪色,C中澄清石灰水变浑浊;(5)答案:B;(6)根据SO2与KMnO4反应的方程式:2KMnO4+5SO2+2H2O=K2SO4+2MnSO4+2H2SO4可知n(