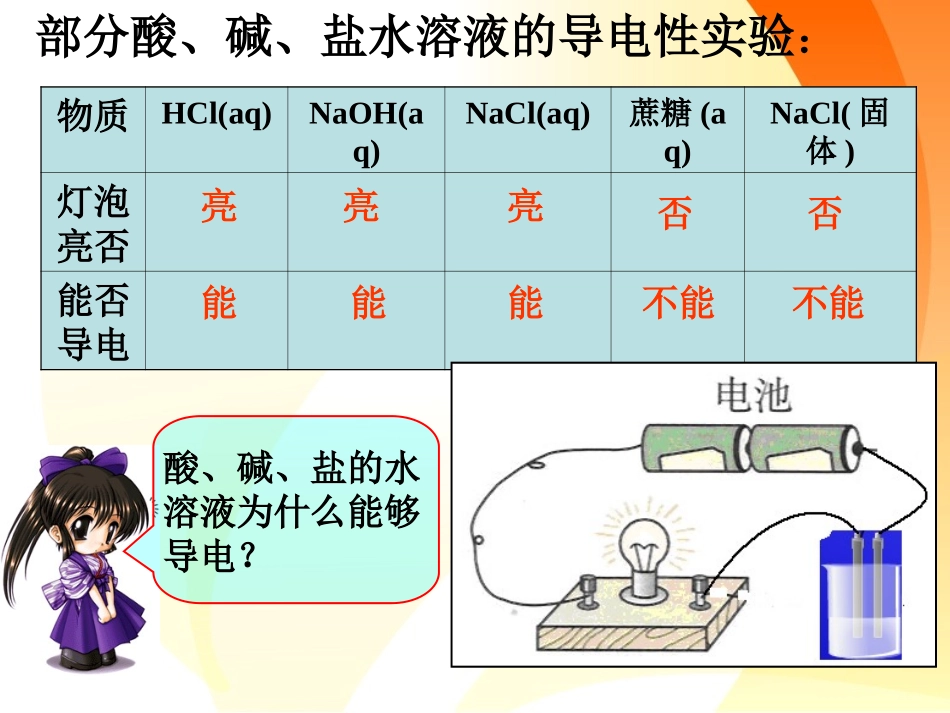
第2节离子反应第1课时酸、碱、盐在水溶液中的电离部分酸、碱、盐水溶液的导电性实验:物质HCl(aq)NaOH(aq)NaCl(aq)蔗糖(aq)NaCl(固体)灯泡亮否能否导电亮亮亮否否能能能不能不能酸、碱、盐的水溶液为什么能够导电
1、电解质在水溶液里或熔融状态下能够导电的化合物叫做电解质
常见的电解质包括酸、碱、盐、活泼金属氧化物、H2O等
2、非电解质在水溶液里和熔融状态下都不能导电的化合物叫做非电解质
常见的非电解质包括NH3、非金属氧化物、大多数有机物等
讨论讨论下列物质哪些是电解质
哪些是非电解质
①CO2、②H2SO4、③Ba(OH)2固体、④Cu、⑤HCl、⑥NaCl溶液、⑦蔗糖、⑧CH3CH2OH、⑨CaSO4答案:电解质:②③⑤⑨,非电解质:①⑦⑧
在理解电解质、非电解质的概念时应该注意:①电解质和非电解质应是化合物;②电解质应是在一定条件下本身电离而导电的化合物
③电解质的判断与物质的溶解性无关
强调强调课堂练习课堂练习下列叙述正确的是()①HCl在水溶液中能够导电,所以HCl是电解质
②固体NaOH不导电,但NaOH是电解质
③NaCl溶液能够导电,所以NaCl溶液是电解质
④CO2溶于水能够导电,所以CO2是电解质
⑤铜能导电,所以铜是电解质
⑥BaSO4不溶于水,所以BaSO4不是电解质
①②①电解质必须是化合物,金属单质(如Al、Fe、Cu)和石墨单质,虽然能够导电,但不是电解质,也不是非电解质
NaCl溶液虽然能够导电,但NaCl溶液是混合物,所以NaCl溶液既不是电解质也不是非电解质
②电解质概念中“溶解”“熔融”两个条件,满足其一即可称为电解质
如BaSO4在水溶液中难导电,但在熔融状态下能导电,所以BaSO4是电解质
分析分析③某些化合物,如CO2、NH3,它们的水溶液能够导电,但不是电解质,因为真正导电的物质是它们与水反应的产物,而不