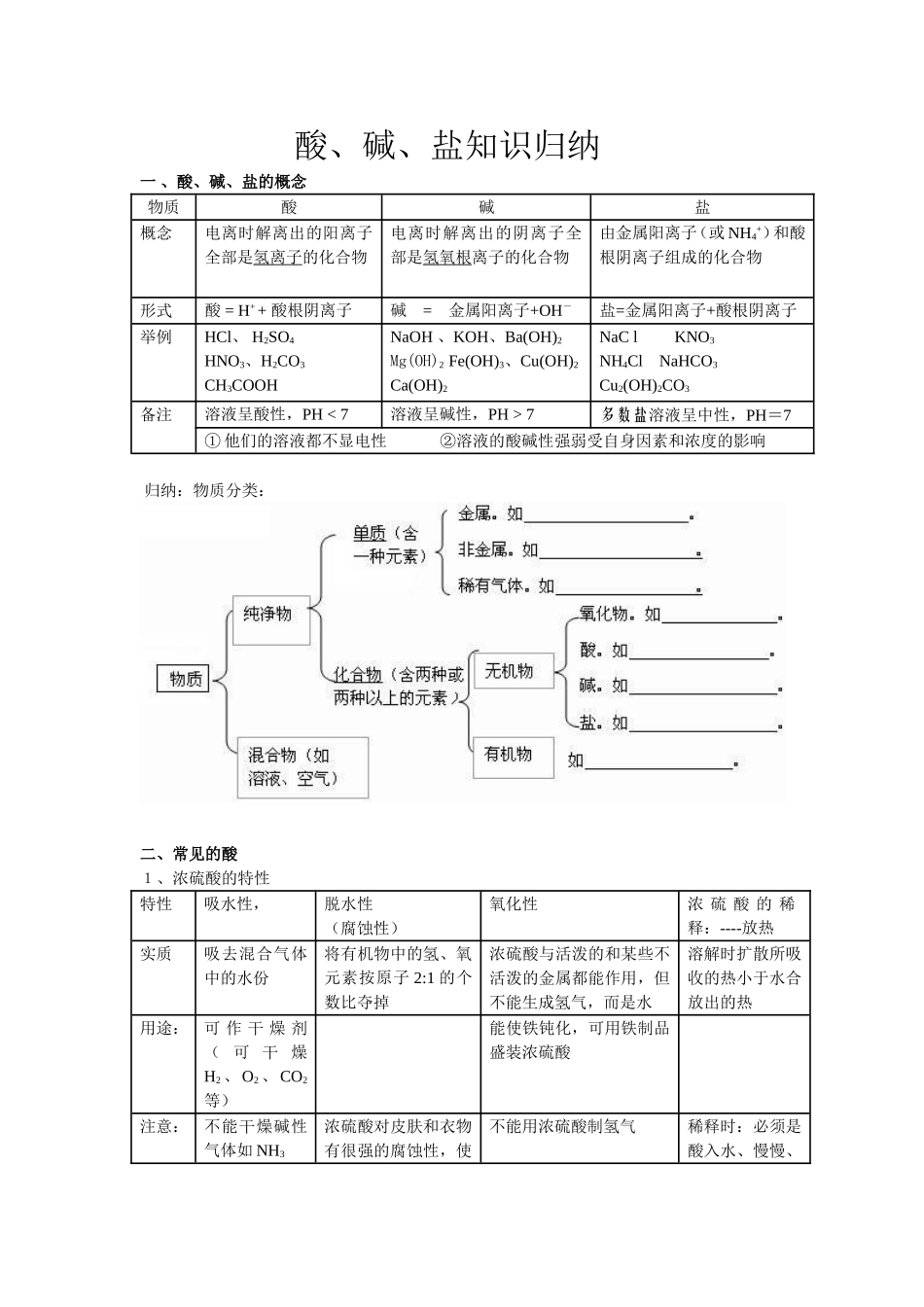
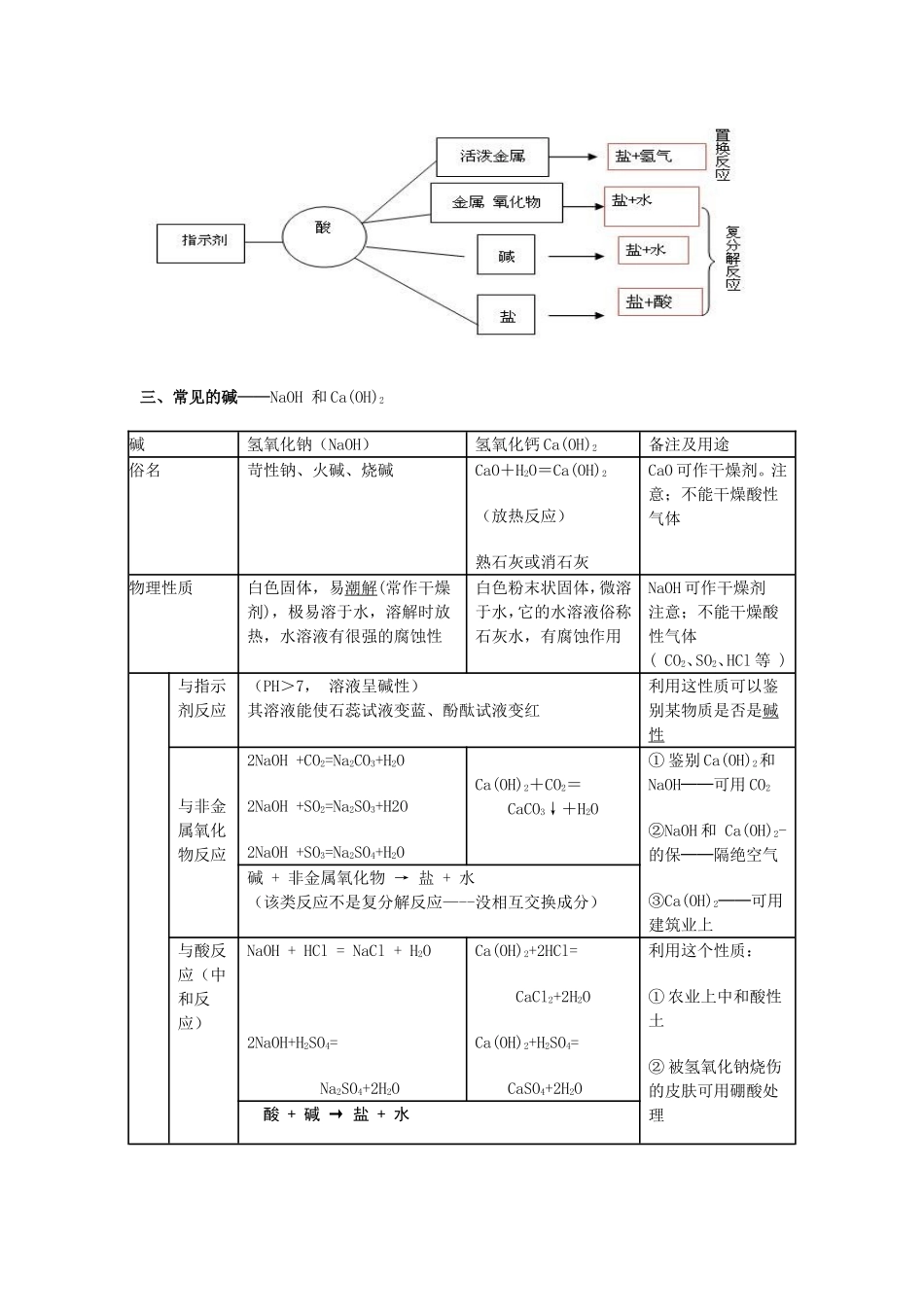
酸、碱、盐知识归纳一、酸、碱、盐的概念物质酸碱盐概念电离时解离出的阳离子全部是氢离子的化合物电离时解离出的阴离子全部是氢氧根离子的化合物由金属阳离子(或NH4+)和酸根阴离子组成的化合物形式酸=H++酸根阴离子碱=金属阳离子+OH-盐=金属阳离子+酸根阴离子举例HCl、H2SO4HNO3、H2CO3CH3COOHNaOH、KOH、Ba(OH)2Mg(OH)2Fe(OH)3、Cu(OH)2Ca(OH)2NaClKNO3NH4ClNaHCO3Cu2(OH)2CO3备注溶液呈酸性,PH7多数盐溶液呈中性,PH=7①他们的溶液都不显电性②溶液的酸碱性强弱受自身因素和浓度的影响归纳:物质分类:二、常见的酸1、浓硫酸的特性特性吸水性,脱水性(腐蚀性)氧化性浓硫酸的稀释:----放热实质吸去混合气体中的水份将有机物中的氢、氧元素按原子2:1的个数比夺掉浓硫酸与活泼的和某些不活泼的金属都能作用,但不能生成氢气,而是水溶解时扩散所吸收的热小于水合放出的热用途:可作干燥剂(可干燥H2、O2、CO2等)能使铁钝化,可用铁制品盛装浓硫酸注意:不能干燥碱性气体如NH3浓硫酸对皮肤和衣物有很强的腐蚀性,使不能用浓硫酸制氢气稀释时:必须是酸入水、慢慢、用时一定要小心
搅拌2、常见的酸──盐酸和稀硫酸酸盐酸(HCl)硫酸(H2SO4)备注及用途物理性质无色液体,易挥发,有刺激性气味,在空气中形成白雾(盐酸越浓越易挥发)无色液体,无挥发性,无气味浓度越大,其密度就越大化学性质1
跟指示剂的反应(PH