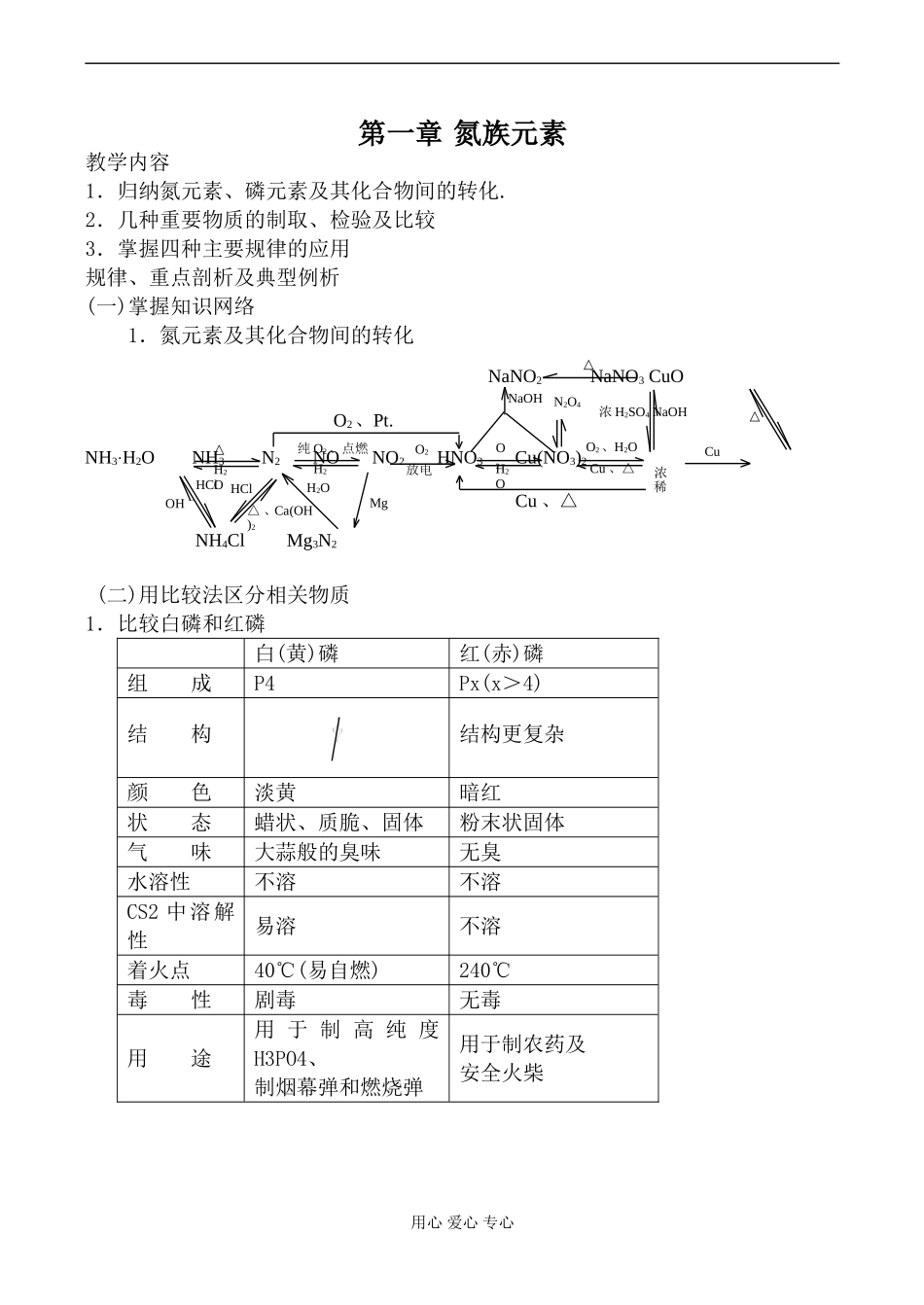
第一章氮族元素教学内容1.归纳氮元素、磷元素及其化合物间的转化
2.几种重要物质的制取、检验及比较3.掌握四种主要规律的应用规律、重点剖析及典型例析(一)掌握知识网络1.氮元素及其化合物间的转化(二)用比较法区分相关物质1.比较白磷和红磷白(黄)磷红(赤)磷组成P4Px(x>4)结构结构更复杂颜色淡黄暗红状态蜡状、质脆、固体粉末状固体气味大蒜般的臭味无臭水溶性不溶不溶CS2中溶解性易溶不溶着火点40℃(易自燃)240℃毒性剧毒无毒用途用于制高纯度H3PO4、制烟幕弹和燃烧弹用于制农药及安全火柴用心爱心专心△△H2O纯O2、点燃H2O2放电O2H2OO2、H2OCu、△CuO2、Pt
浓稀Cu、△NaNO2NaNO3CuONaOHN2O4浓H2SO4NaOHMgHClHClOH-△、Ca(OH)2H2O△NH4ClMg3N2NH3·H2ONH3N2NONO2HNO3Cu(NO3)2相互转变保存水封密闭密封2.NO、NO2、N2O4的性质及转化NONO2N2O4颜色无色红棕色无色毒性有有有水溶性难易且反应随NO2与H2O反应,平衡不断移动与O2是否共存否能能相互转化(三)抓住典型物质的结构、性质、用途、制取等内在关系1.氮气物性难溶于水熔沸点很低N2无色无气味气体2.氨的结构和性质分子式电子式结构式用心爱心专心白磷红磷260℃416℃升华、冷凝均要隔绝空气NO2NOH2O或SO2N2O4N非极性分子分子晶体N≡N叁键键能大:N::N:
固定常温:很难反应(作保护气)高温(或放电):也能反应(制NH3、HNO3)氮的化合态氧化性N2+3H22NH3高温、高压催化剂3Mg+N2Mg3N2点燃化性用途还原性N2+O22NO放电表示式33HNH:N:HHHHH特点-3价为N最低价有孤对电子极性分子(三角锥形)性质有还原性与H+等形成配位键极易溶于水(1:700)反应:4NH3+5O