氯气的生产原理【教学目标】了解氯碱工业的基本原理和方法、氯气的实验室制备
【教学重点】氯碱工业的基本原理【教学难点】氯碱工业的基本流程
【教学方法】参观访问、观看录像与自学相结合
【教学过程】〖引入〗人们如何从海水中获取氯化钠并使用氯化钠
一、氯碱工业:以电解食盐水为基础制取氯气等产品的工业
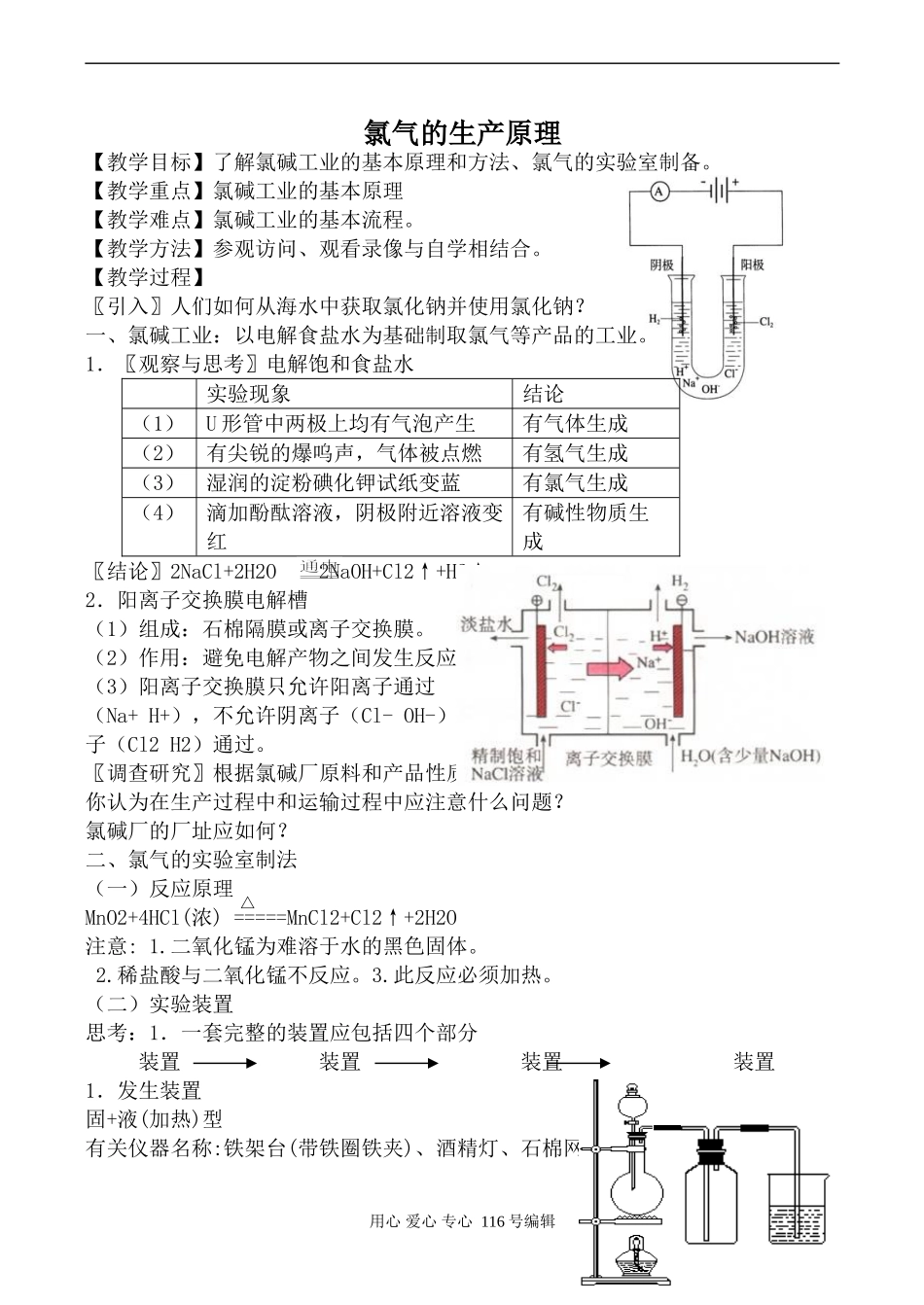
1.〖观察与思考〗电解饱和食盐水实验现象结论(1)U形管中两极上均有气泡产生有气体生成(2)有尖锐的爆呜声,气体被点燃有氢气生成(3)湿润的淀粉碘化钾试纸变蓝有氯气生成(4)滴加酚酞溶液,阴极附近溶液变红有碱性物质生成〖结论〗2NaCl+2H2O2NaOH+Cl2↑+H2↑2.阳离子交换膜电解槽(1)组成:石棉隔膜或离子交换膜
(2)作用:避免电解产物之间发生反应
(3)阳离子交换膜只允许阳离子通过(Na+H+),不允许阴离子(Cl-OH-)和分子(Cl2H2)通过
〖调查研究〗根据氯碱厂原料和产品性质,你认为在生产过程中和运输过程中应注意什么问题
氯碱厂的厂址应如何
二、氯气的实验室制法(一)反应原理MnO2+4HCl(浓)=====MnCl2+Cl2↑+2H2O注意:1
二氧化锰为难溶于水的黑色固体
稀盐酸与二氧化锰不反应
此反应必须加热
(二)实验装置思考:1.一套完整的装置应包括四个部分装置装置装置装置1.发生装置固+液(加热)型有关仪器名称:铁架台(带铁圈铁夹)、酒精灯、石棉网、用心爱心专心116号编辑△烧瓶、双孔塞、分液漏斗、玻璃导管
装配原则:自下而上思考:1.本实验装置有何不足
2.制取氯气的过程中可能产生哪些杂质气体,如何除去
2.净化装置3.气体收集和尾气处理装置1.氯气比空气重且能溶于水,应用什么方法收集
2.氯气有毒,不能排放到空气中,应如何处理
实验室制备氯气的装置图思考:仪器的装配原则
(三)氯气的检验:氯气可用湿润的淀粉-碘化钾试纸放在集气瓶口检