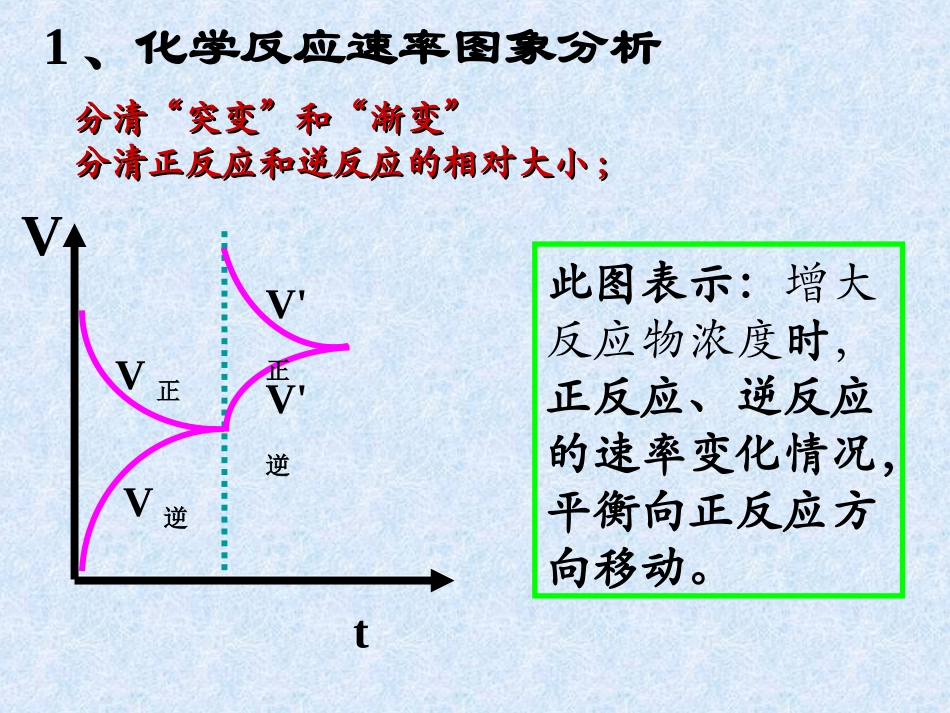
化学反应速率和化学平衡的图象分清“突变”和“渐变”分清“突变”和“渐变”分清正反应和逆反应的相对大小分清正反应和逆反应的相对大小;;此图表示:增大反应物浓度时,正反应、逆反应的速率变化情况,平衡向正反应方向移动
1、化学反应速率图象分析V正V逆V'正V'逆VtV正V逆V'正V'逆tV答:从逆反应开始
平衡向正反应方向移动
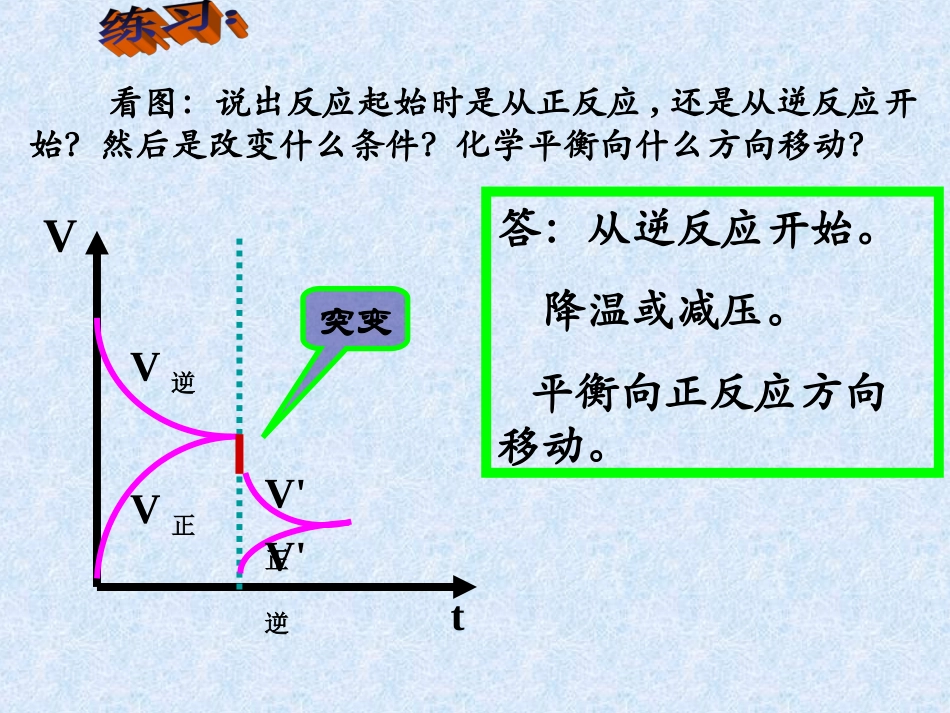
看图:说出反应起始时是从正反应,还是从逆反应开始
然后是改变什么条件
化学平衡向什么方向移动
突变V正V逆V'正V'逆=tV看图:说出反应起始时是从正反应;还是从逆反应开始
然后是改变什么条件
化学平衡向什么方向移动
突变答:正、逆反应同时开始
加催化剂平衡不移动
或者是对于反应前后体积不变的反应,增大压强起始量不为0例例11可逆反应3A(g)+3B(g)C(g)在其他条件不变时,随着反应进行温度(T)对C物质的量的影响如图所示.下列说法正确的是()A、t1时,T2或T2条件下反应都处于平衡状态B、T1<T2,△H<0C、T1>T2,△H>0D、若改变压强平衡不发生移动1T2T1t反应时间tn(C)0B解题原则:(1)先拐先平,数值大B(A)达到平衡后,若使用催化剂,C的质量分数增大(B)平衡后,若升高温度,则平衡向逆反应方向移动(C)平衡后,增大A的量,有利于平衡正向移动(D)化学方程式中一定有n>p+q练习、可逆反应mA(s)+nB(g)pC(g)+qD(g)
反应中,当其它条件不变时,C的质量分数与温度(T)和压强(P)的关系如下图,根据图中曲线分析,判断下列叙述中正确的是()例2:可逆反应:aX(s)+bY(g)cZ(g)+dW(g)达到平衡,混合物中Y的体积分数随压强(P)与温度T(T2>T1)的变化关系如图示
1、当压强不变时,升高温度,Y的体积分数变___,平衡向______方向移动,则正反应是____热反应
2、当温度不变时,增