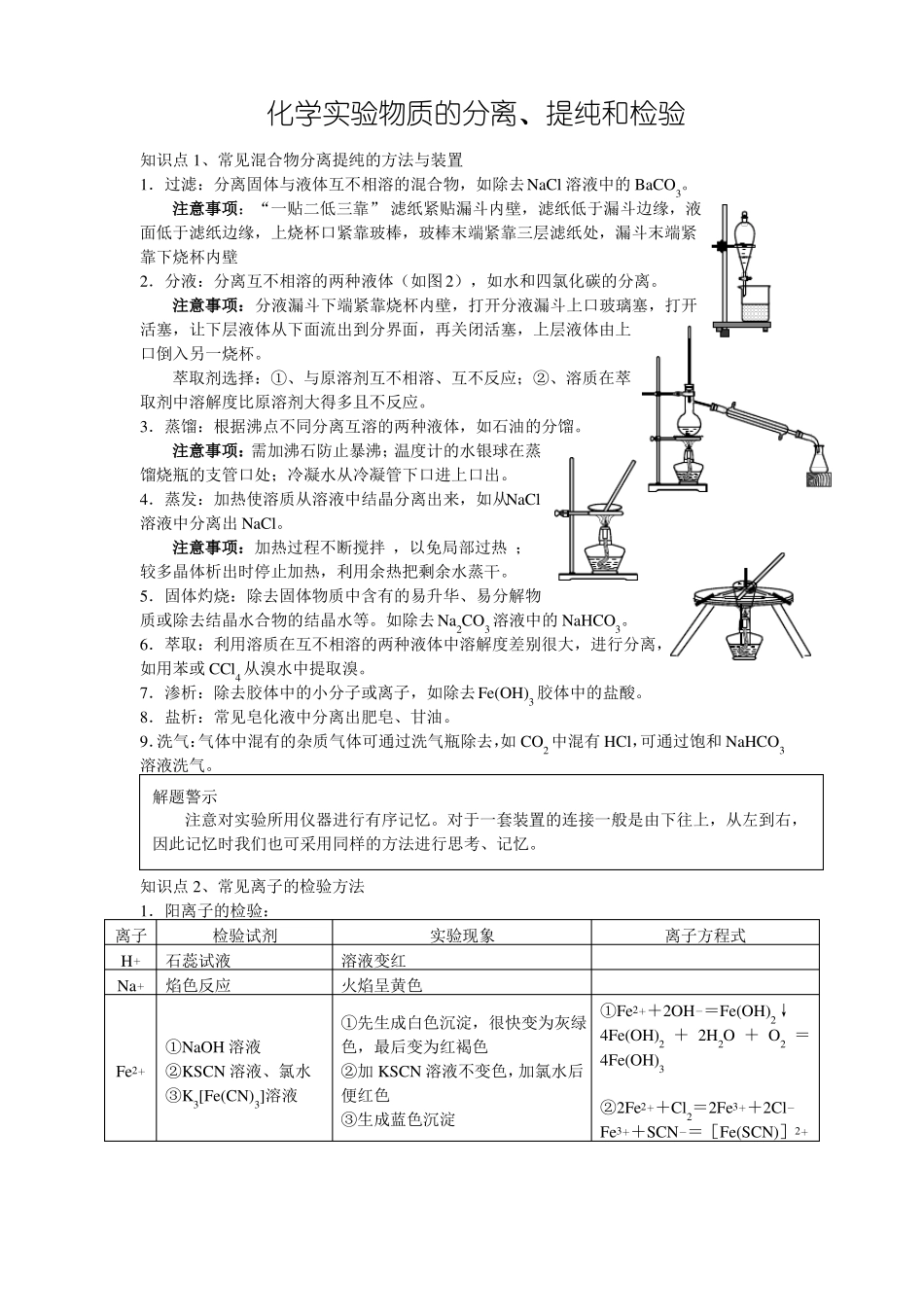
化学实验物质的分离、提纯和检验知识点1、常见混合物分离提纯的方法与装置1.过滤:分离固体与液体互不相溶的混合物,如除去NaCl溶液中的BaCO3
注意事项:“一贴二低三靠”滤纸紧贴漏斗内壁,滤纸低于漏斗边缘,液面低于滤纸边缘,上烧杯口紧靠玻棒,玻棒末端紧靠三层滤纸处,漏斗末端紧靠下烧杯内壁2.分液:分离互不相溶的两种液体(如图2),如水和四氯化碳的分离
注意事项:分液漏斗下端紧靠烧杯内壁,打开分液漏斗上口玻璃塞,打开活塞,让下层液体从下面流出到分界面,再关闭活塞,上层液体由上口倒入另一烧杯
萃取剂选择:①、与原溶剂互不相溶、互不反应;②、溶质在萃取剂中溶解度比原溶剂大得多且不反应
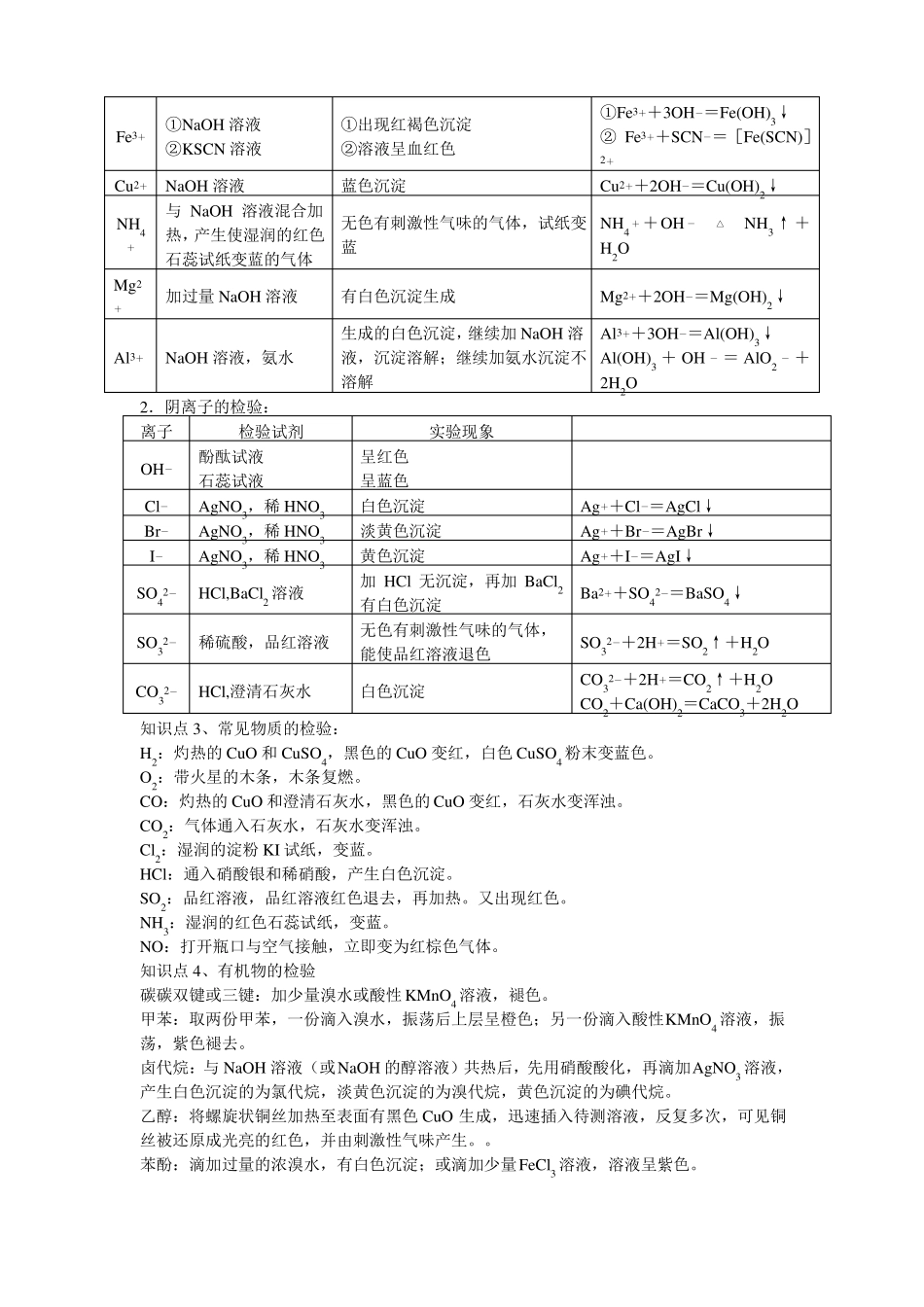
3.蒸馏:根据沸点不同分离互溶的两种液体,如石油的分馏
注意事项:需加沸石防止暴沸;温度计的水银球在蒸馏烧瓶的支管口处;冷凝水从冷凝管下口进上口出
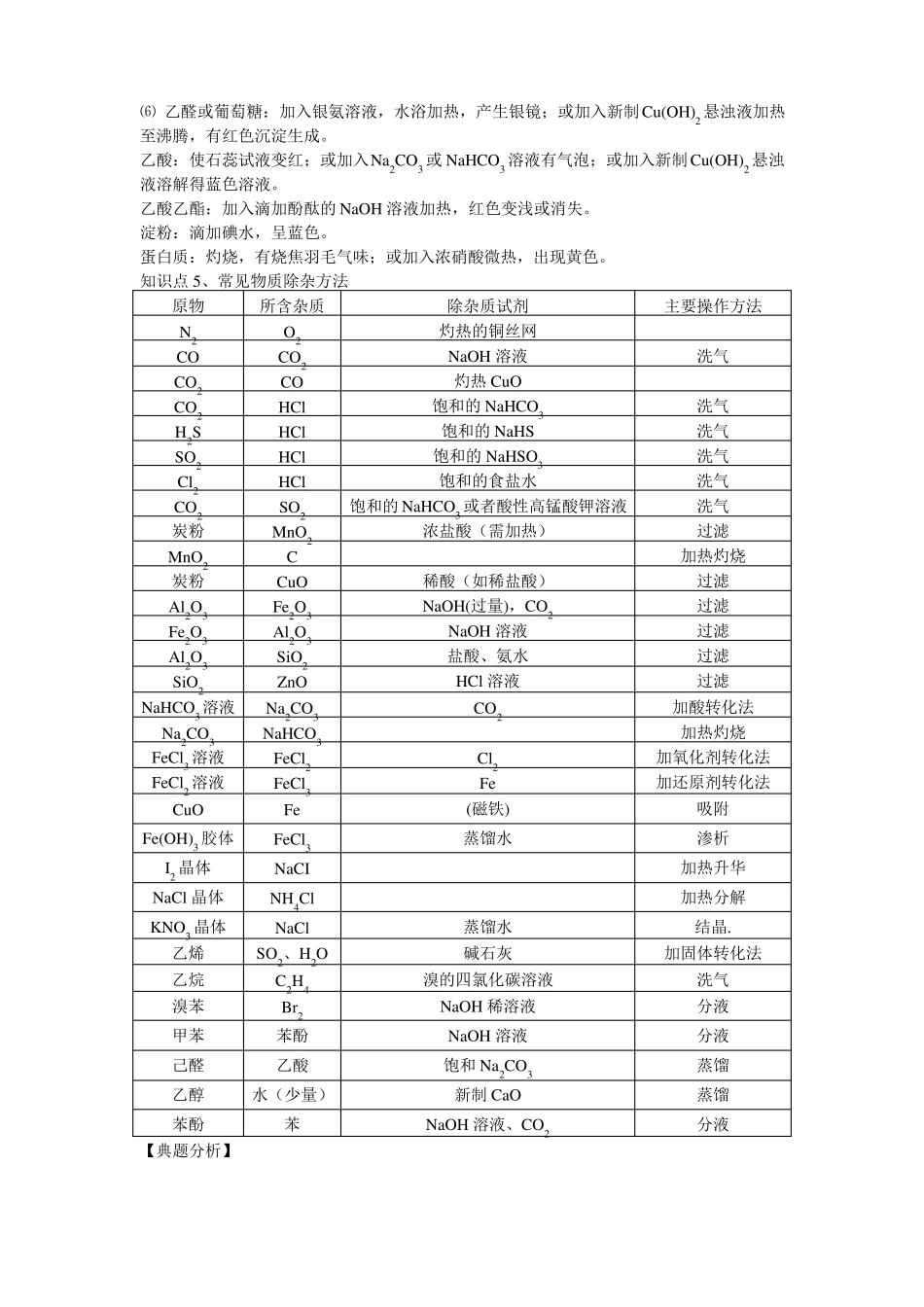
4.蒸发:加热使溶质从溶液中结晶分离出来,如从NaCl溶液中分离出NaCl
注意事项:加热过程不断搅拌,以免局部过热;较多晶体析出时停止加热,利用余热把剩余水蒸干
5.固体灼烧:除去固体物质中含有的易升华、易分解物质或除去结晶水合物的结晶水等
如除去Na2CO3溶液中的NaHCO3
6.萃取:利用溶质在互不相溶的两种液体中溶解度差别很大,进行分离,如用苯或CCl4从溴水中提取溴
7.渗析:除去胶体中的小分子或离子,如除去Fe(OH)3胶体中的盐酸
8.盐析:常见皂化液中分离出肥皂、甘油
9.洗气:气体中混有的杂质气体可通过洗气瓶除去,如CO2中混有HCl,可通过饱和NaHCO3溶液洗气
解题警示注意对实验所用仪器进行有序记忆
对于一套装置的连接一般是由下往上,从左到右,因此记忆时我们也可采用同样的方法进行思考、记忆
知识点2、常见离子的检验方法1.阳离子的检验:离子HNa++检验试剂石蕊试液焰色反应溶液变红火焰呈黄色实验现象离子方程式+-①Fe2+2O