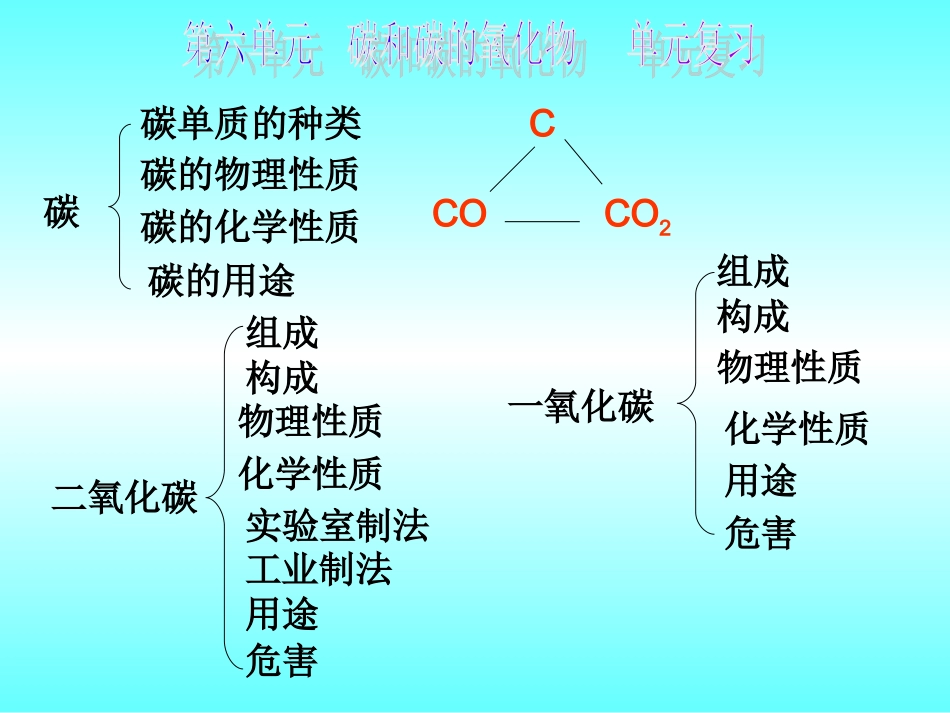
碳碳单质的种类碳的物理性质碳的化学性质碳的用途二氧化碳物理性质化学性质用途实验室制法工业制法危害一氧化碳物理性质化学性质用途危害组成构成组成构成CCOCO2碳碳碳的物理性质:碳的物理性质:碳单质的种类碳单质的种类金刚石:金刚石:石墨:石墨:CC6060无色透明的正八面体,无色透明的正八面体,最硬。最硬。深灰黑色细磷片状固体,深灰黑色细磷片状固体,最软最软,是,是电和热的良导体,有润滑性。电和热的良导体,有润滑性。碳的化学性质:碳的化学性质:11、常温下稳定、常温下稳定22、具有可燃性、具有可燃性33、具有还原性、具有还原性C+OC+O22=CO=CO22((OO22充充足)足)点燃2C+O2C+O22=2CO=2CO((OO22不不足)足)点燃C+2CuO=2Cu+CO2↑高温用途用途金刚石金刚石作装饰品、玻璃刀、钻探机的钻头作装饰品、玻璃刀、钻探机的钻头石墨石墨作铅笔芯、电极、高温润滑剂作铅笔芯、电极、高温润滑剂活性炭活性炭作净水剂、防毒面具、防溴鞋垫、脱色剂;作净水剂、防毒面具、防溴鞋垫、脱色剂;炭黑炭黑作鞋油、颜料、墨水;作鞋油、颜料、墨水;焦炭焦炭冶炼金属。冶炼金属。物理性质:通常情况下,二氧化碳是无色无味的气体,密度比空气大,可溶于水。固态叫二氧化碳(干冰),易升华。化学性质:1、二氧化碳既不燃烧也不支持燃烧。2、能与石灰水反应:CO2+Ca(OH)2=CaCO3↓+H2O3、能与水反应:CO2+H2O=H2CO3对环境的影响1、用途:光合作用(气体肥料)、灭火、制冷剂、人工降雨、化工产品的原料2、危害(1)过量损害人体健康。10%可使人窒息死亡。(2)温室效应组成:二氧化碳是由碳元素和氧元素组成的。构成:二氧化碳是由二氧化碳分子构成,每个二氧化碳分子是由一个碳原子和两个氧原子构成。实验室制法药品:石灰石、稀盐酸原理:CaCO3+2HCl=CaCl2+H2O+CO2↑装置步骤:查、装、加、封、收。工业制法:高温煅烧石灰石CaCO3=CaO+CO2↑高温二氧化碳一氧化碳CO物理性质:无色无味的气体,难溶于水。剧毒。化学性质:(1)具有可燃性(2)具有还原性危害:剧毒,破坏人体的血红蛋白,使人体缺氧死亡。用途:作燃料,冶炼金属2CO+O2=2CO2点燃CO+CuO=Cu+CO2△组成:一氧化碳是由碳元素和氧元素组成的。构成:一氧化碳是由一氧化碳分子构成。每个一氧化碳分子是由一个碳原子和一个氧原子构成。氢气H2物理性质:无色无味的气体,难溶于水,密度比空气小化学性质:(1)具有可燃性(2)具有还原性2H2+O2=2H2O点燃H2+CuO=Cu+H2O△用途:作燃料,冶炼金属可燃性气体点燃之前一定要检验其纯度CCOCO2C+OC+O22=CO=CO22((OO22充充足)足)点燃2C+O2C+O22=2CO=2CO((OO22不不足)足)点燃C+2CuO=2Cu+CO2↑高温CaCO3+2HCl=CaCl2+H2O+CO2↑2CO+O2=2CO2点燃CO+CuO=Cu+CO2△CO2+Ca(OH)2=CaCO3↓+H2OH2O+CO2=H2CO3CaCO3=CaO+CO2↑高温H2CO3=H2O+CO2↑C+CO2=2CO高温CaCO3H2CO3H2、CO、C的区别相似性:H2、CO、C都具有可燃性可燃性和还原还原性性。C+OC+O22=CO=CO22点燃2CO+O2=2CO2点燃CO+CuO=Cu+CO2△2H2+O2=2H2O点燃H2+CuO=Cu+H2O△C+2CuO=2Cu+CO2↑高温氧化还原反应:有氧得失的反应。氧化剂:失去氧的物质。发生还原反应。还原剂:得到氧的物质。发生氧化反应。为什么干冰可用于人工降雨?答:因为干冰易升华,升华时向周围吸收大量的热,使空气中的水蒸气迅速冷凝成水滴,于是开始下雨。进入久未开启的菜窖或干涸的深井、山洞之前要做什么实验?答:做灯火实验。把燃着的火把伸进去,若火焰变暗可熄灭,说明二氧化碳浓度过大,不能进去。什么是温室效应?如何防止温室效应?实验室为什么不用稀硫酸与石灰石反应制取二氧化碳?实验室为什么不用稀盐酸与碳酸钠反应制取二氧化碳?一氧化碳的毒性是什么?家用煤气中含一氧化碳,如发现煤气泄漏应当怎么办?如何证明鸡蛋壳或珍珠贝壳中含有碳酸钙?有一种气体可能是CO、CO2、H2、HCl气体的混合物,依次通过如下装置,现象如下:A中石灰水不变浑浊,C中的黑色粉末变红,D中无水硫酸铜不变色,E中的石灰水变浑浊,假设每一步中气体均反应完全,试推断:混合气体中一定存在,一定不存在,可能存在。无水硫酸铜遇水变蓝,可用于证明水的存在...