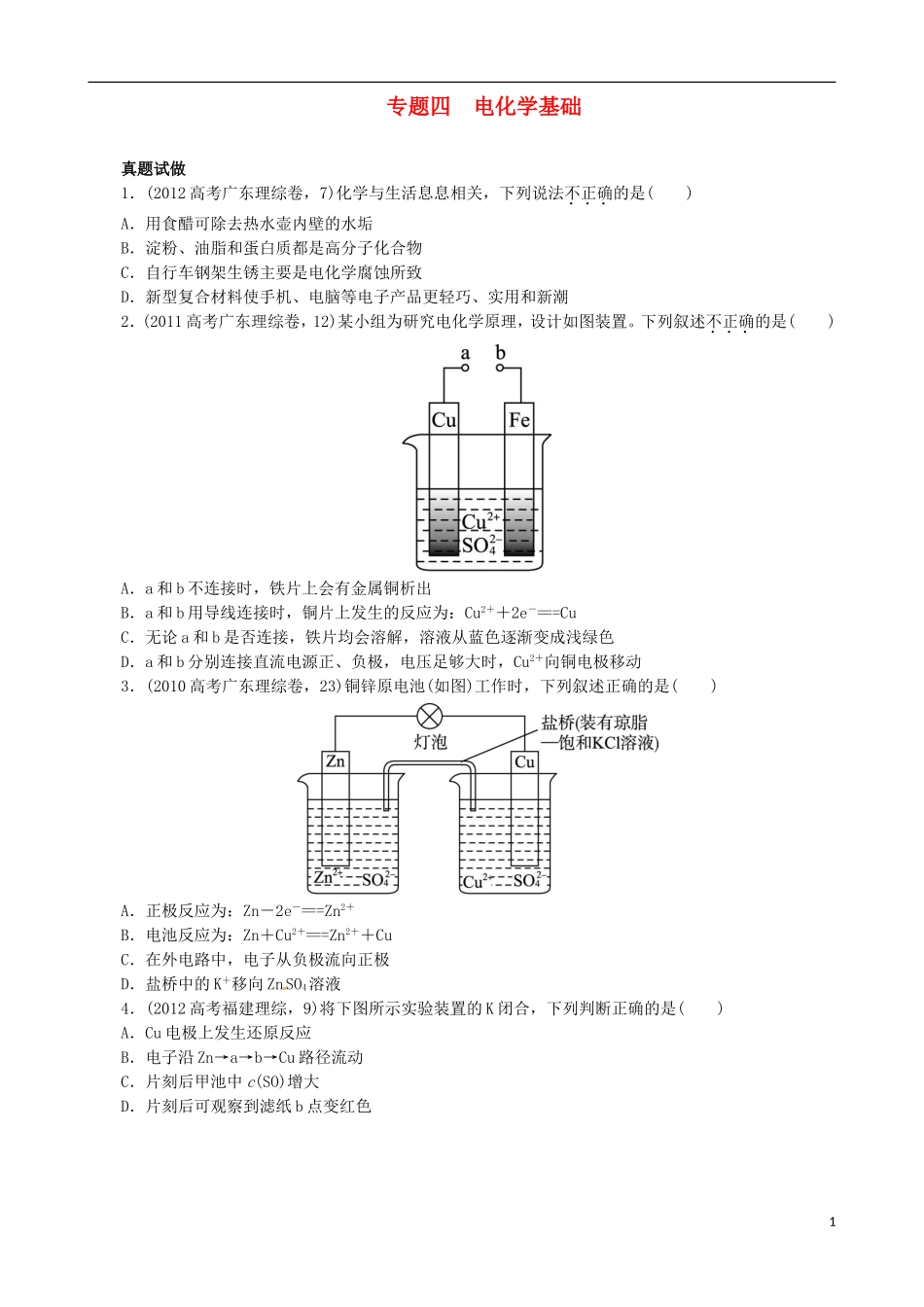
专题四电化学基础真题试做1.(2012高考广东理综卷,7)化学与生活息息相关,下列说法不正确的是()A.用食醋可除去热水壶内壁的水垢B.淀粉、油脂和蛋白质都是高分子化合物C.自行车钢架生锈主要是电化学腐蚀所致D.新型复合材料使手机、电脑等电子产品更轻巧、实用和新潮2.(2011高考广东理综卷,12)某小组为研究电化学原理,设计如图装置
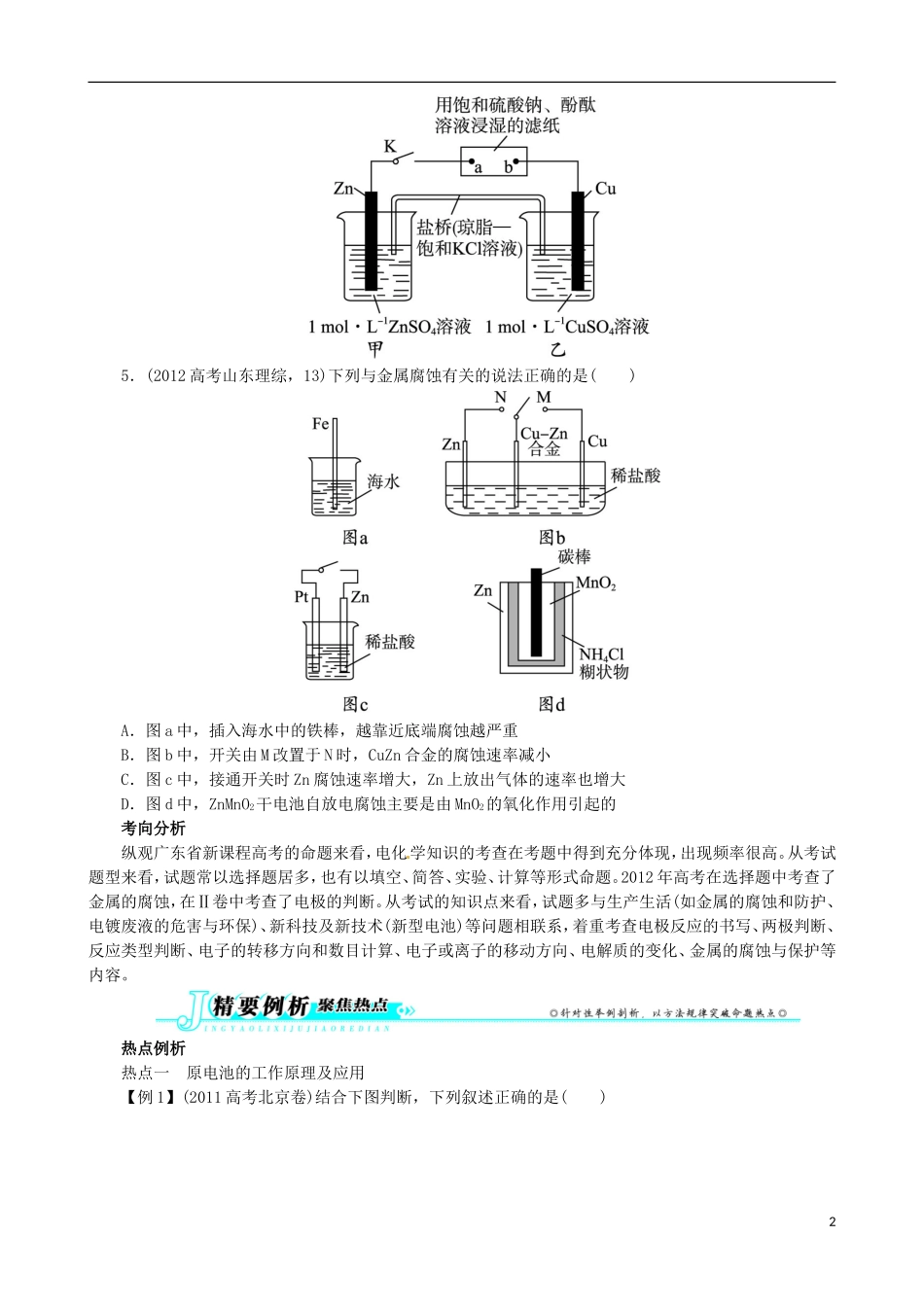
下列叙述不正确的是()A.a和b不连接时,铁片上会有金属铜析出B.a和b用导线连接时,铜片上发生的反应为:Cu2++2e-===CuC.无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成浅绿色D.a和b分别连接直流电源正、负极,电压足够大时,Cu2+向铜电极移动3.(2010高考广东理综卷,23)铜锌原电池(如图)工作时,下列叙述正确的是()A.正极反应为:Zn-2e-===Zn2+B.电池反应为:Zn+Cu2+===Zn2++CuC.在外电路中,电子从负极流向正极D.盐桥中的K+移向ZnSO4溶液4.(2012高考福建理综,9)将下图所示实验装置的K闭合,下列判断正确的是()A.Cu电极上发生还原反应B.电子沿Zn→a→b→Cu路径流动C.片刻后甲池中c(SO)增大D.片刻后可观察到滤纸b点变红色15.(2012高考山东理综,13)下列与金属腐蚀有关的说法正确的是()A.图a中,插入海水中的铁棒,越靠近底端腐蚀越严重B.图b中,开关由M改置于N时,CuZn合金的腐蚀速率减小C.图c中,接通开关时Zn腐蚀速率增大,Zn上放出气体的速率也增大D.图d中,ZnMnO2干电池自放电腐蚀主要是由MnO2的氧化作用引起的考向分析纵观广东省新课程高考的命题来看,电化学知识的考查在考题中得到充分体现,出现频率很高
从考试题型来看,试题常以选择题居多,也有以填空、简答、实验、计算等形式命题
2012年高考在选择题中考查了金属的腐蚀,在Ⅱ卷中考查了电极的判断