http://www
e-huaxue
com版权所有第一节化学反应与能量的变化教学目标:知识与技能:1
使学生了解化学反应中能量转化的原因和常见的能量转化形式;2
认识化学反应过程的物质变化和能量变化;3
了解反应热和焓变的涵义;4
能正确认识、书写热化学方程式
过程与方法:1
通过对学习资料的查找与交流,培养学生获取信息、理解信息并得出结论的能力以及语言表达能力;2
通过从化学键的角度分析化学反应,引导学生分析引起反应热的本质
情感态度与价值观:培养学生从微观的角度理解化学问题
教学重点、难点:1
化学反应中的能量变化及其微观原因2
正确认识、书写热化学方程式教学方式:课外资料及生活中的化学现象引入,由宏观到微观,揭示实质,引导、结合练习
教学过程:一、反应热焓变:在化学反应过程中放出或吸收的热量、通常叫做反应热
(1)符号:用△H表示
(2)单位:一般采用kJ/mol
(3)可直接测量,测量仪器叫量热计
(4)研究对象:一定压强下,在敞口容器中发生的反应所放出或吸收的热量
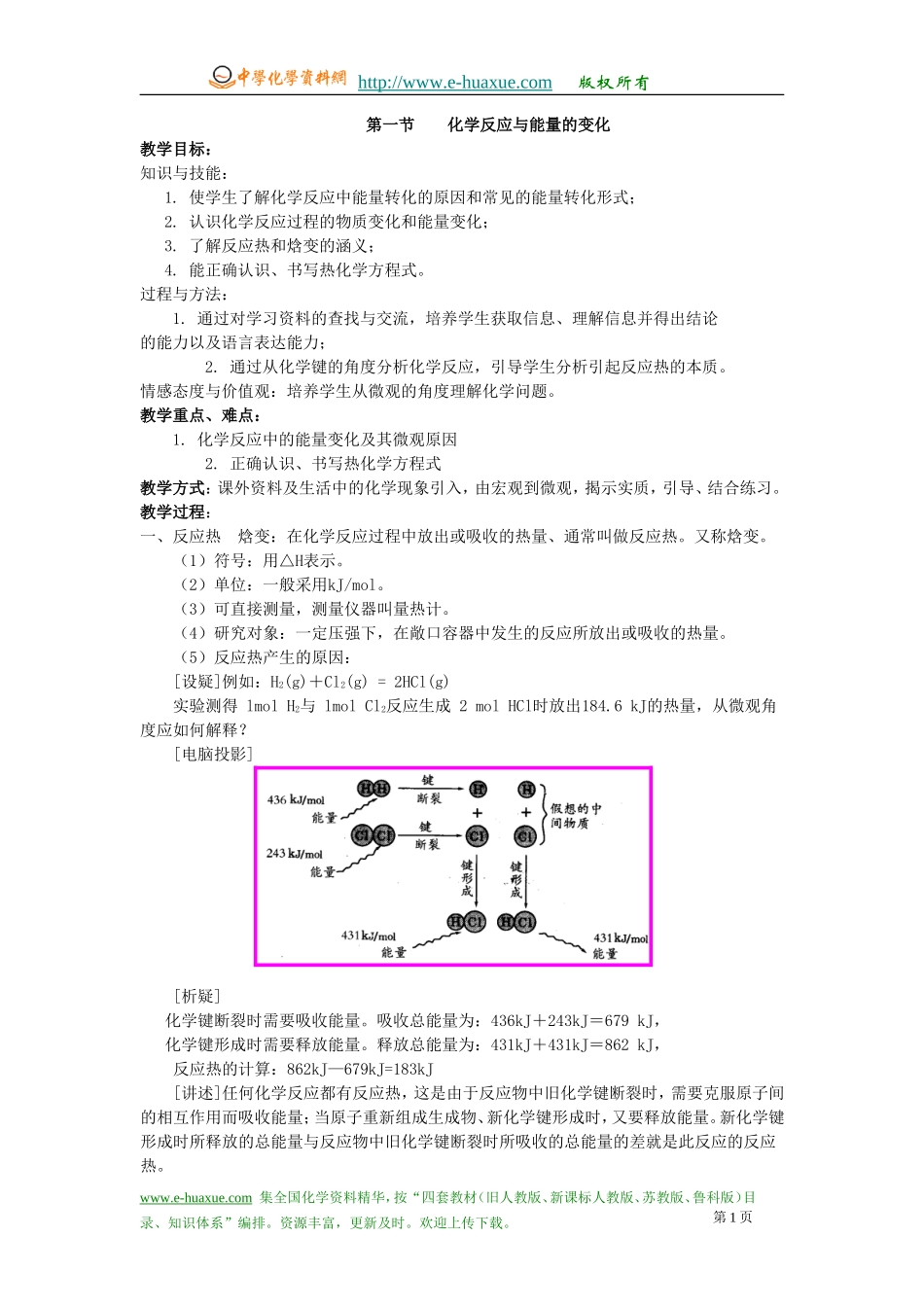
(5)反应热产生的原因:[设疑]例如:H2(g)+Cl2(g)=2HCl(g)实验测得lmolH2与lmolCl2反应生成2molHCl时放出184
6kJ的热量,从微观角度应如何解释
[电脑投影][析疑]化学键断裂时需要吸收能量
吸收总能量为:436kJ+243kJ=679kJ,化学键形成时需要释放能量
释放总能量为:431kJ+431kJ=862kJ,反应热的计算:862kJ—679kJ=183kJ[讲述]任何化学反应都有反应热,这是由于反应物中旧化学键断裂时,需要克服原子间的相互作用而吸收能量;当原子重新组成生成物、新化学键形成时,又要释放能量
新化学键形成时所释放的总能量与反应物中旧化学键断裂时所吸收的总能量的差就是此反应的反应热
e-huaxue
com集全国化学资料精华