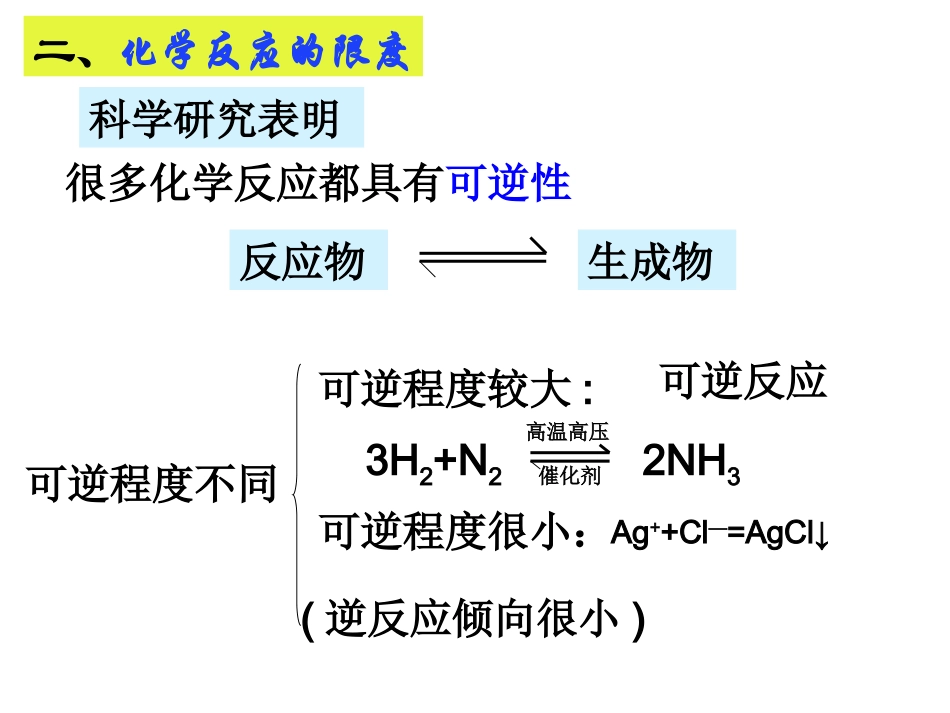
化学反应限度科学研究表明很多化学反应都具有可逆性反应物生成物可逆程度不同可逆程度很小:(逆反应倾向很小)可逆程度较大:可逆反应二、化学反应的限度3H2+N22NH3高温高压催化剂Ag++Cl—=AgCl↓可逆反应:在相同条件下能向正、反两个方向同时进行的化学反应称为可逆反应
反应不能进行到底反应不能进行到底((反应物和生成物同时存在反应物和生成物同时存在))特征•同一条件,正反应和逆反应同时进行[思考1]在一定条件下把3摩尔氢气和1摩尔氮气置于容积为1升的密闭容器中,反应过程中N2、H2、NH3浓度变化情况填入下表,最终能生成2摩尔NH3
C(N2)C(H2)C(NH3)起始最大最大O过程减少减少增大N2(g)+3H2(g)2NH3(g)正向反应逆向反应(4)随着反应的进行,v(正)与v(逆)怎样变化
在密闭容器中加入1molN2和1molH2发生反应(1)当反应刚开始时,反应物和生成物的浓度哪个大
(3)当反应刚开始时,正反应速率与逆反应速率哪个大
(2)随着反应的进行,反应物和生成物浓度如何变化
二、化学反应的限度反应速率v(正)v(逆)v(正)=v(逆)t1时间(t)0(1)0~t1:v(正)>v(逆)(2)t1以后:v(正)=v(逆)(1)t1时刻以后反应物和生成物浓度如何变化
问题:(2)反应是不是停止了
(一)化学平衡状态在一定条件下的可逆反应里,正反应和逆反应的速率相等,反应物和生成物浓度不再改变时的状态
二、化学反应的限度(1)逆:可逆反应特征(4)定:反应物和生成物浓度保持恒定不变(3)动:动态平衡v(正)=v(逆)≠0(2)等:v(正)=v(逆)(5)变:条件改变,平衡状态可能发生改变平衡状态是可逆反应在一定条件下能达到(或完成)的最大限度
课堂作业1、对化学反应限度的叙述,错误的()A.任何可逆反应都有一定的限度B.化学反应达到限度时,正逆反应速率相等