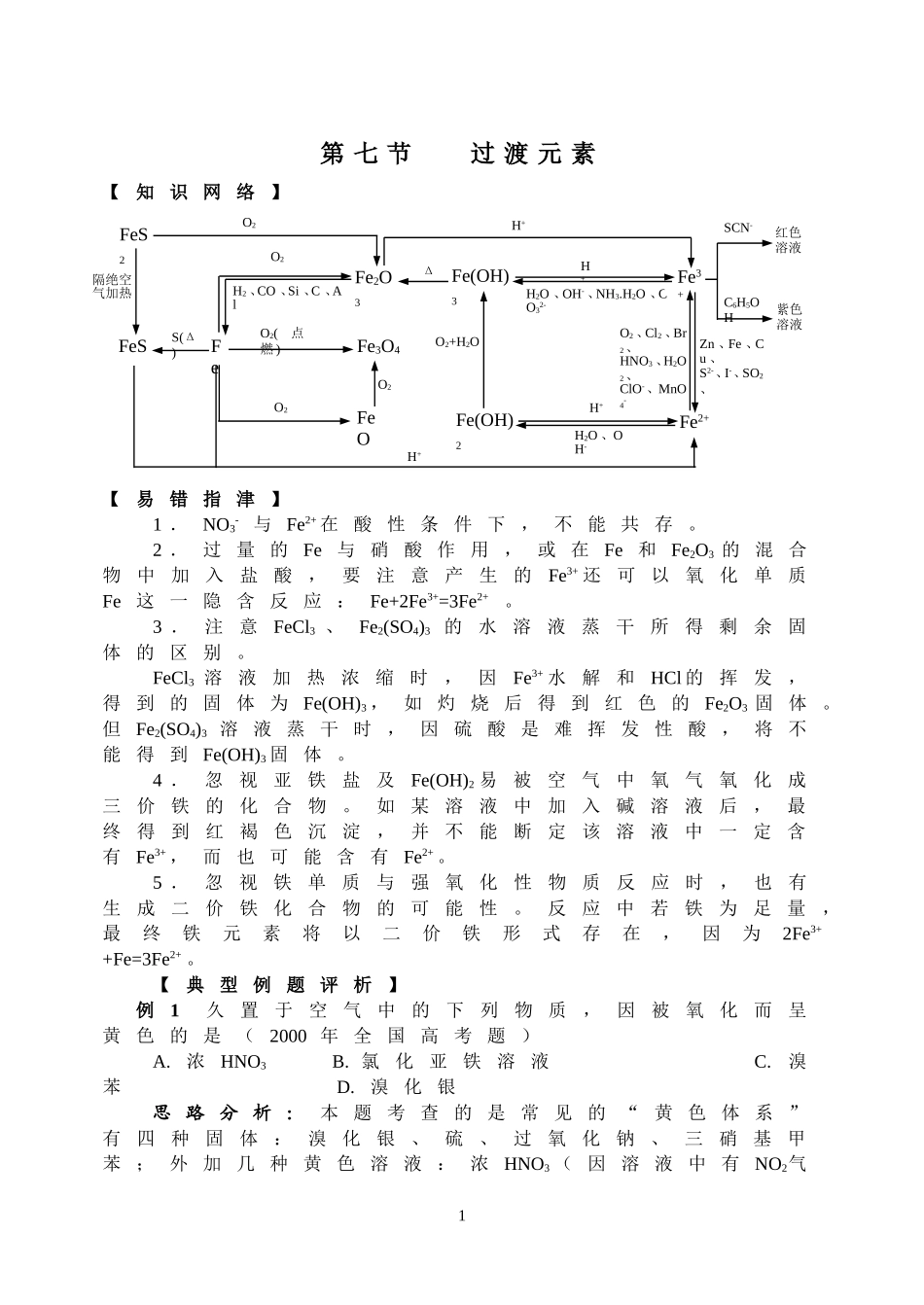
第七节过渡元素【知识网络】【易错指津】1.NO3-与Fe2+在酸性条件下,不能共存
2.过量的Fe与硝酸作用,或在Fe和Fe2O3的混合物中加入盐酸,要注意产生的Fe3+还可以氧化单质Fe这一隐含反应:Fe+2Fe3+=3Fe2+
3.注意FeCl3、Fe2(SO4)3的水溶液蒸干所得剩余固体的区别
FeCl3溶液加热浓缩时,因Fe3+水解和HCl的挥发,得到的固体为Fe(OH)3,如灼烧后得到红色的Fe2O3固体
但Fe2(SO4)3溶液蒸干时,因硫酸是难挥发性酸,将不能得到Fe(OH)3固体
4.忽视亚铁盐及Fe(OH)2易被空气中氧气氧化成三价铁的化合物
如某溶液中加入碱溶液后,最终得到红褐色沉淀,并不能断定该溶液中一定含有Fe3+,而也可能含有Fe2+
5.忽视铁单质与强氧化性物质反应时,也有生成二价铁化合物的可能性
反应中若铁为足量,最终铁元素将以二价铁形式存在,因为2Fe3++Fe=3Fe2+
【典型例题评析】例1久置于空气中的下列物质,因被氧化而呈黄色的是(2000年全国高考题)A
浓HNO3B
氯化亚铁溶液C
溴化银思路分析:本题考查的是常见的“黄色体系”有四种固体:溴化银、硫、过氧化钠、三硝基甲苯;外加几种黄色溶液:浓HNO3(因溶液中有NO2气1隔绝空气加热紫色溶液红色溶液H+O2SCN-O2+H2OC6H5OHH2O、OH-H+H2O、OH-、NH3
H2O、CO32-O2H2、CO、Si、C、AlFeFeSFe2O3Fe3O4FeOFe(OH)2Fe(OH)3FeS2S(Δ)Fe3+Fe2+Zn、Fe、Cu、S2-、I-、SO2、O2、Cl2、Br2、HNO3、H2O2、ClO-、MnO4-O2O2(点燃)O2ΔH+H+体)、工业盐酸(含Fe3+离子)、不纯的硝基苯(因溶有NO2)、亚铁盐溶液(因含Fe3+离子)等
对于该题除考查物质的物理性