http://www
e-huaxue
com版权所有第二节燃烧热能源教学目标:1
了解燃烧热概念,并能进行简单的计算
知道化学反应中能量转化的原因,能说出常见的能量转化形式
通过查阅资料说明能源是人类生存和发展的重要基础,了解化学在解决能源危机中的重要作用
知道节约能源、提高能量利用效率的实际意义
教学重点、难点:燃烧热概念及相关计算
教学过程:复习热化学方程式的意义,书写热化学方程式的注意事项,引入新课
一、燃烧热反应热种类:燃烧热、中和热、溶解热等1.定义:在101kPa时,lmol物质完全燃烧生成稳定的氧化物时所放出的热量,叫做该物质的燃烧热
[学生讨论、归纳概念要点](1)在101kPa时,生成稳定的氧化物
如C完全燃烧应生成CO2(g),而生成CO(g)属于不完全燃烧
又如H2燃烧生成液态H2O,而不是气态水蒸气
(2)燃烧热通常是由实验测得的
(3)可燃物以lmol作为标准进行测量
(4)计算燃烧热时,热化学方程式常以分数表示
例:H2(g)十O2(g)=H2O(l);△H=-285
8kJ/mol2.研究物质燃烧热的意义了解化学反应完成时产生热量的多少,以便更好地控制反应条件,充分利用能源
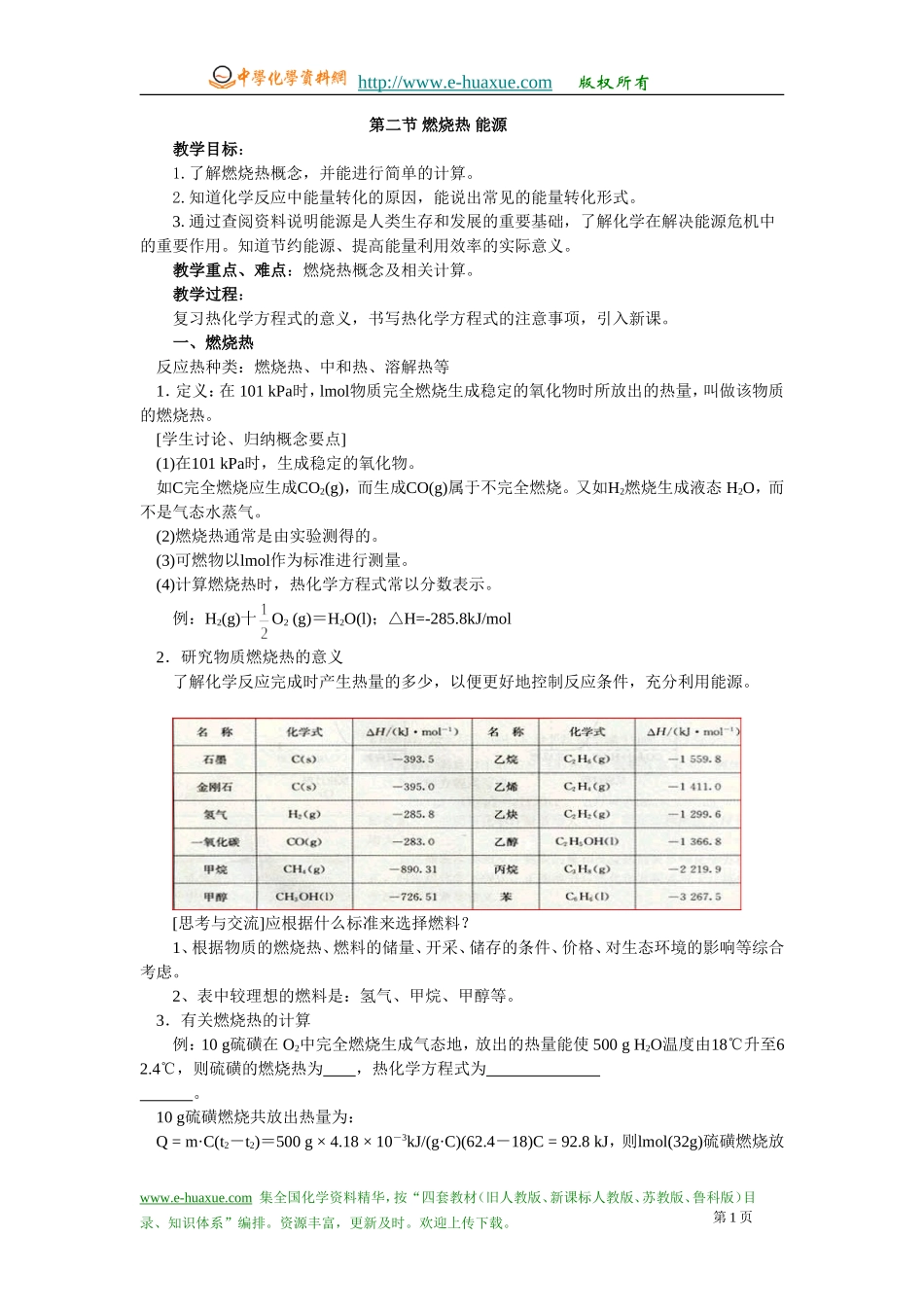
[思考与交流]应根据什么标准来选择燃料
1、根据物质的燃烧热、燃料的储量、开采、储存的条件、价格、对生态环境的影响等综合考虑
2、表中较理想的燃料是:氢气、甲烷、甲醇等
3.有关燃烧热的计算例:10g硫磺在O2中完全燃烧生成气态地,放出的热量能使500gH2O温度由18℃升至62
4℃,则硫磺的燃烧热为,热化学方程式为
10g硫磺燃烧共放出热量为:Q=m·C(t2-t2)=500g×4
18×10-3kJ/(g·C)(62
4-18)C=92
8kJ,则lmol(32g)硫磺燃烧放www
e-huaxue
com集全国化学资料精华,按“四套教材(旧人教版、新课标人