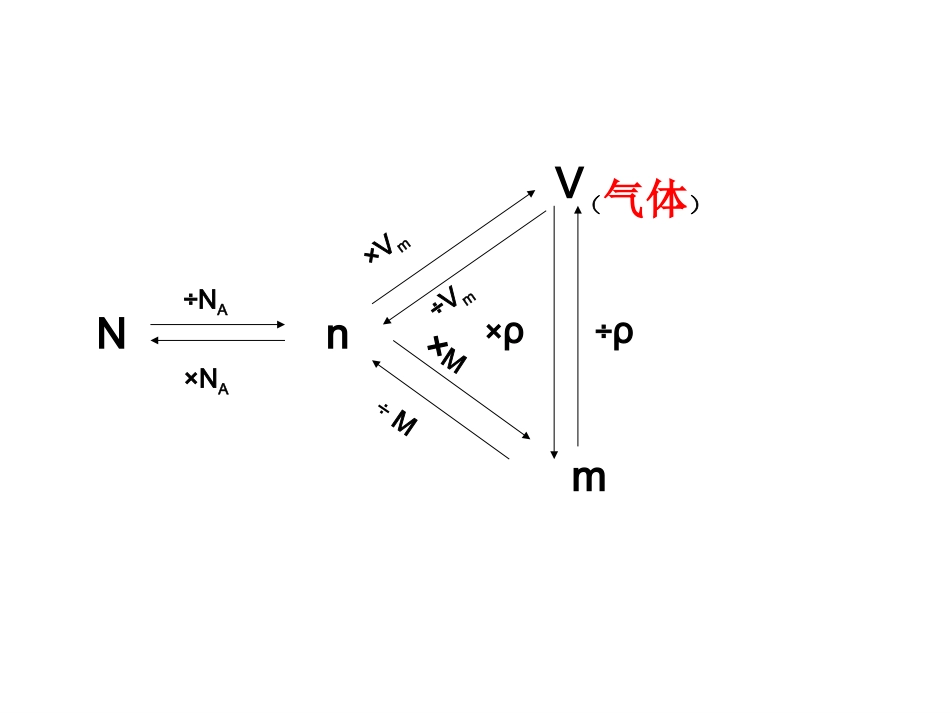
阿伏加德罗定律推论及应用阿伏加德罗定律推论及应用Vm(气体)nN÷NA×NA×Vm÷Vm×M÷M×ρ÷ρ0
02mol某气体的质量为0
88g,该气体的摩尔质量为_______,那么在标准状况下,它的体积是_________,密度为_______
练一练练一练44g·mol-10
96g·L-1其中:P——压强,V——体积,n——物质的量,T——温度,R——常数气体方程:PV=nRT或PV=—RTmM介绍推论1
同温同压下,气体体积之比等于物质的量之比——=——=——(T,P一定)n2V2V1n1N1N2一
阿伏加德罗定律的推论:依据:PV=nRT或PV=—RTmM1
同温同压下,相同体积的下列气体中,质量最大的是()(A)氯气(B)氢气(C)氧气(D)氮气2
同温同压下,同物质的量的CH4气体与CO体积比是()(A)3:1(B)1:1(C)1:3(D)2:3练一练练一练AB推论2
同温同压下,任何气体密度比等于摩尔质量(式量)之比——=——ρ1ρ2M1M2(P,T一定)依据:PV=nRT或PV=—RTmM1
同温同压下,等质量的二氧化硫和二氧化碳相比较,下列叙述中,正确的是()(A)密度比为16:11(B)密度比为11:16(C)体积比为1:1(D)体积比为11:162
在相同温度和压强下,下列气体密度最小的是()A
Cl2练一练练一练ADB推论3
同温同体积下,气体的压强之比等于物质的量之比————=————=————P1P2n1n2N1N2(T
V一定)依据:PV=nRT或PV=—RTmM1
同温同体积下,相同压强的氢气和甲烷的原子个数之比是()A
1:8A练一练练一练2
一个密闭容器中盛有11gCO2时,压强为1×104Pa
如果在相同温度下,把更多的CO2充入容器中,使容器内压强增至5×104Pa