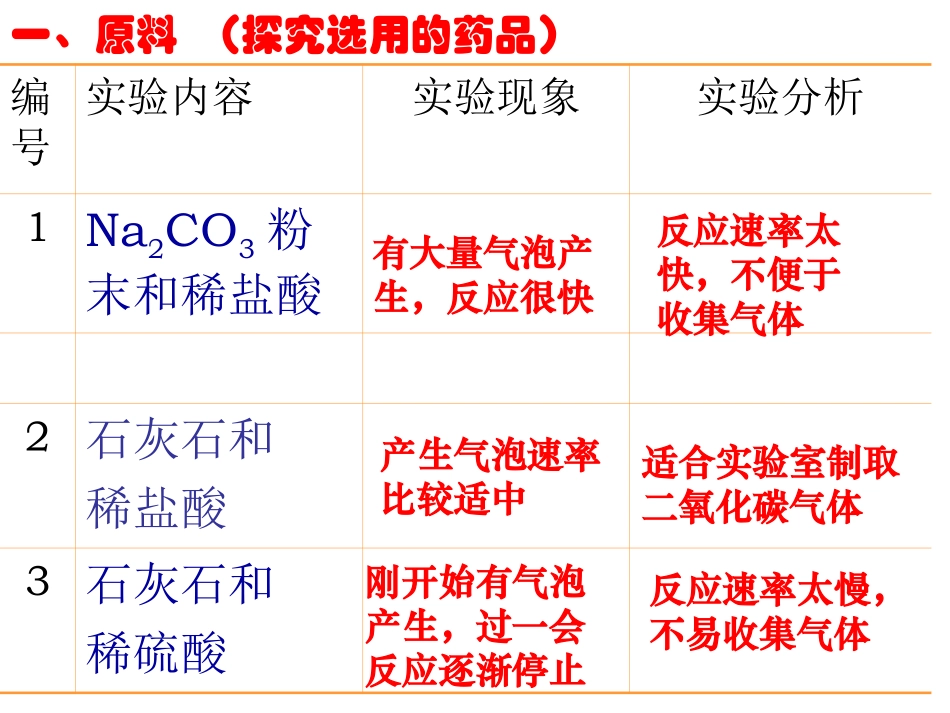
课题2二氧化碳制取的研究一、原料(探究选用的药品)编号实验内容实验现象实验分析1Na2CO3粉末和稀盐酸2石灰石和稀盐酸3石灰石和稀硫酸有大量气泡产生,反应很快反应速率太快,不便于收集气体产生气泡速率比较适中适合实验室制取二氧化碳气体刚开始有气泡产生,过一会反应逐渐停止反应速率太慢,不易收集气体实验1:稀盐酸与碳酸钠粉未反应现象分析结论反应非常剧烈,短时间产生大量气泡碳酸钠粉未的表面积很大,与盐酸接触面积大,反应速度很快,不易控制反应,不便于收集气体实验室不能用稀盐酸与碳酸钠粉未反应来制取二氧化碳该反应的化学方程式为:Na2CO3+2HCl=2NaCl+H2O+CO2实验室制取二氧化碳的反应原理实验2:稀盐酸与石灰石反应我们通过下面三个对比实验进行探亲究注意观察反应现象,并分析原因,然后填写下表现象分析有大量气泡产生,石灰石逐渐溶解该反应在常温下进行,反应速度适中,便于控制
石灰石与稀盐酸反应生成了碳酸和氯化钙:CaCO3+2HCl=CaCl2+H2CO3碳酸很不稳定,分解成水和二氧化碳:H2CO3=H2O+CO2总反应方程式为:CaCO3+2HCl=CaCl2+H2O+CO2实验3:稀硫酸与石灰石反应现象分析刚开始有大量气泡产生,一时间后,气泡逐渐减少,反应逐渐停止
虽然该反应能生成二氧化碳:CaCO3+H2SO4==CaSO4+H2O+CO2但生成的CaSO4微溶于水,它覆盖在石灰石表面,使石灰石与酸不能继续接触,反应会逐渐停止
结论实验室制取二氧化碳能不能用稀硫酸代替稀盐酸二、反应原理:CaCO3+2HCl=CaCl2+H2O+CO2↑制取二氧化碳药品选取原则是:①反应条件是否容易达到;②产生气体的量是多少;③收集的气体是否纯净;④装置、操作是否简单;⑤原料是否易得、价廉
一、原料:实验室制取二氧化碳常用石灰石和稀盐酸或大理石和稀盐酸实验室制取气体的装置气体发生装置气