浓度/mol·L-1时间/s0
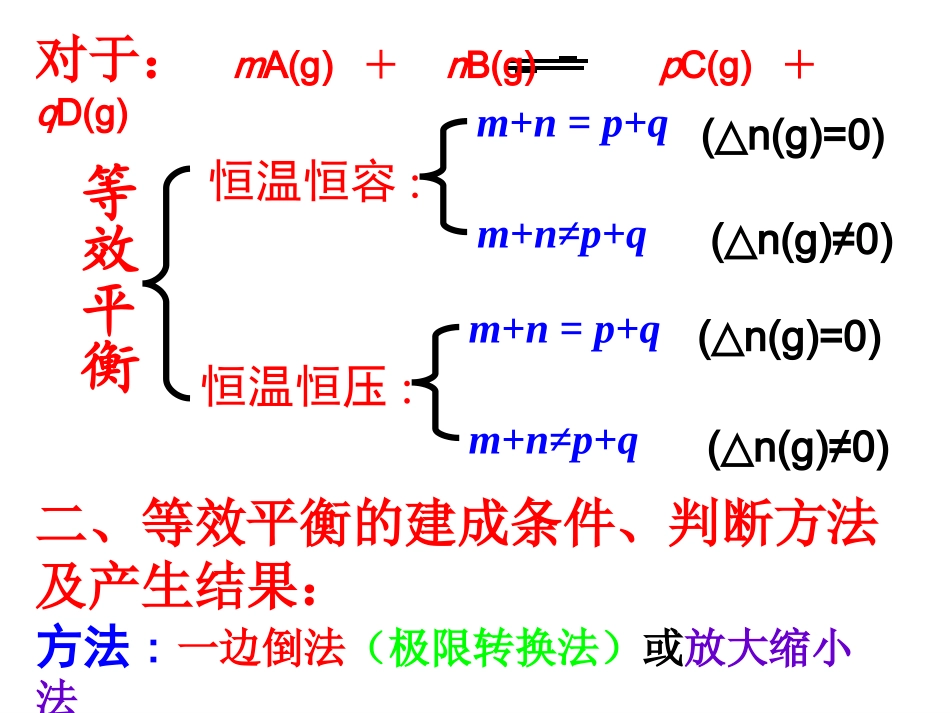
21浓度/mol·L-1t2HIH2或I20
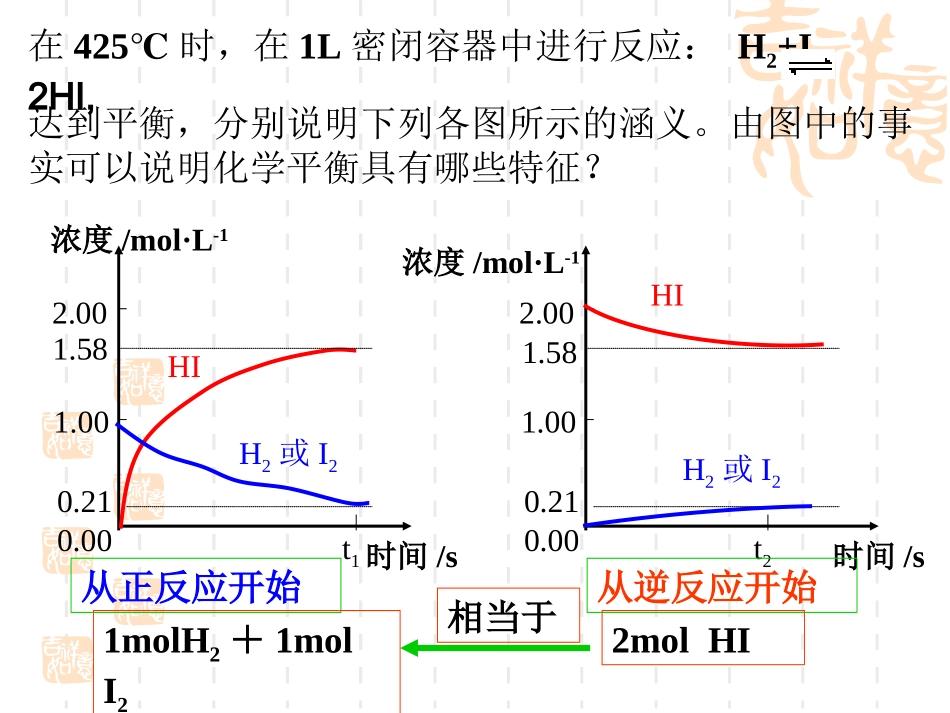
21t1时间/sHIH2或I2从正反应开始从逆反应开始1molH2+1molI22molHI相当于在425℃时,在1L密闭容器中进行反应:H2+I22HI,达到平衡,分别说明下列各图所示的涵义
由图中的事实可以说明化学平衡具有哪些特征
一、等效平衡的概念:在相同条件下,同一可逆反应无论从正反应开始,还是从逆反应开始,还是从既有反应物又有生成物开始,达到化学平衡时,只要各组分(同种物质比较)的百分含量(如物质的量分数)相同,这样的平衡称为等效平衡
等效平衡专题等效平衡恒温恒容:m+n=p+qm+n≠p+q恒温恒压:m+n=p+qm+n≠p+q对于:mA(g)+nB(g)pC(g)+qD(g)(n(g)=0)△(n(g)=0)△(n(g)≠0)△(n(g)≠0)△二、等效平衡的建成条件、判断方法及产生结果:方法:一边倒法(极限转换法)或放大缩小法(一)恒温恒容1:(n△(g)≠0)2SO2+O2催化剂加热2SO3SO2a%O2b%SO3c%平衡状态ⅠSO2a%O2b%SO3c%SO2a%O2b%SO3c%平衡状态ⅡSO2a%O2b%SO3c%平衡状态Ⅱ
2molSO21molO2A2molSO21molO2B2molSO21molO2B4molSO22molO2BSO2a%O2b%SO3c%平衡状态Ⅱ恒温恒容(n△(g)≠0)SO2a%O2b%SO3c%平衡状态2molSO21molO2A2molSO21molO2B2molSO21molO2B4molSO22molO2B2molSO21molO2B2molSO21molO2B4molSO22molO2B非等效平衡
2SO2+O2催化剂加热2SO3方法:放大缩小法(一)、等效平衡建成条件探