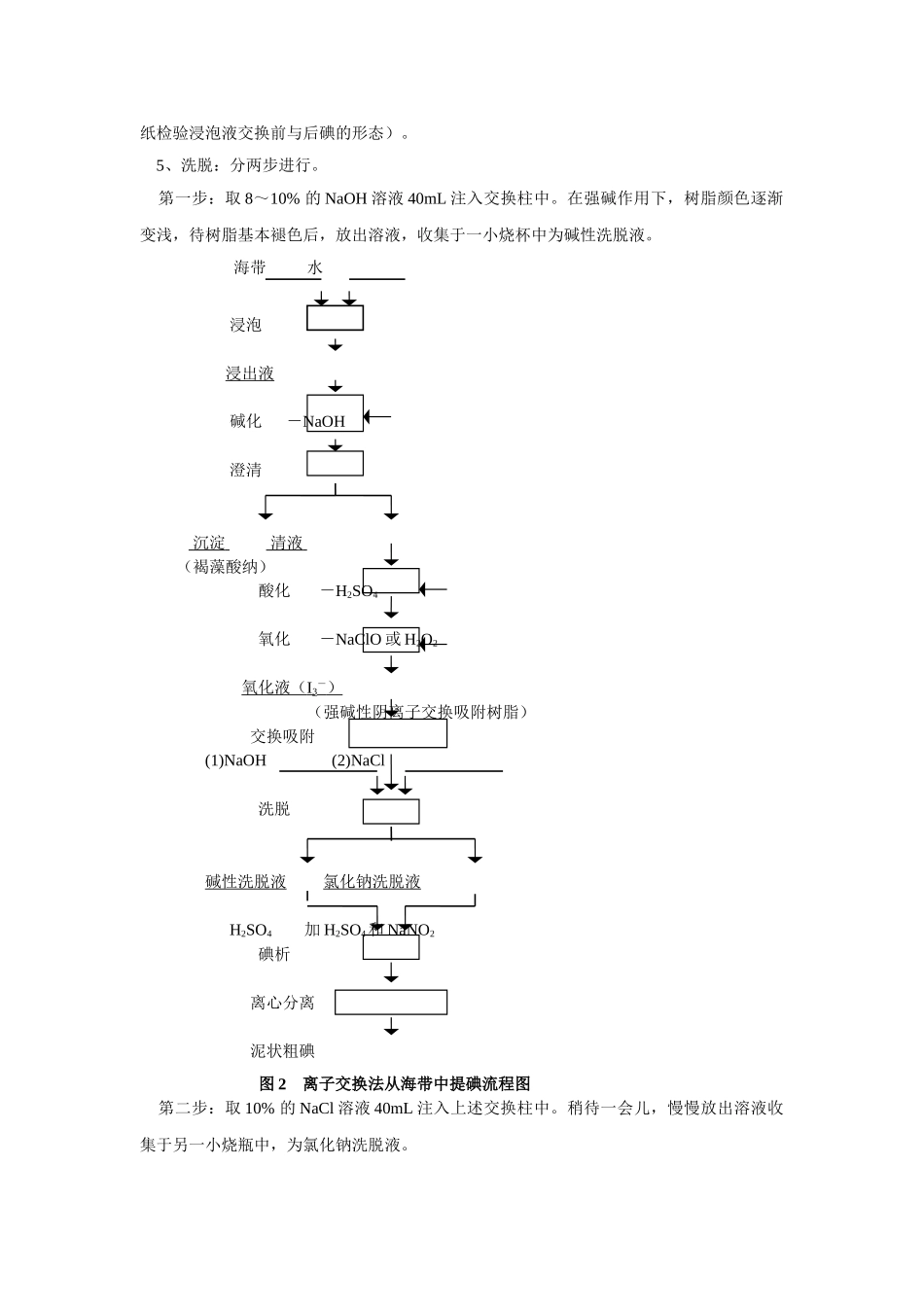
实验八用离子交换法从海带中提碘一、目的要求:用离子交换法从海带中提碘涉及一系列物理化学过程,有助于学生理解卤素单质及化合物的氧化还原性,了解歧化反应的实用意义,并能初步掌握离子交换剂应用技术
二、方法概述:海带中所含的碘一般以I-离子状态存在
用水浸泡海带,I-离子及其它可溶性有机质如褐藻糖胶等进入浸出液中
若用海带重量13-15倍的水量浸泡海带,可使浸出液中I-离子含量达到0
海带浸出液中褐藻糖胶的存在妨碍碘的提取,应预先除去
一般采用碱化絮凝法使其生成褐藻酸钠絮状沉淀而沉降
由于强碱性阴离子交换树脂对多碘离子I3-或I5-离子的交换吸附量(700~800克/升树脂)远远大于对I-离子的吸附量(150~170克/升树脂),因此常将海带浸出液中的I-离子部分氧化使生成I3-或I5-离子,再被树脂交换吸附
一般采用在酸性条件下加入适量氧化剂,如NaClO或H2O2的方法使I-离子氧化并生成多碘离子以利于交换吸附,氧化及交换反应方程式如下:2I-+ClO-+2H+=I2+Cl-+H2O或2I-+2H++H2O2=I2+2H2OI2+I-=I3-R-Cl+I3-=R-I3+Cl-吸附碘达饱和的树脂呈黑红色
先后用氢氧化钠溶液及氯化钠溶液处理树脂,可以将碘洗脱
氢氧化钠溶液洗脱碘主要是发生了歧化反应,洗脱液中含有I-和IO3-离子:3R-I3+6NaOH=3R-I+5NaI+NaIO3+3H2O氯化钠溶液洗脱碘则是发生了如下的交换反应,I-离子进入洗脱液中,树脂同时被再生为氯型:R-I+NaCl=R-Cl+NaI往碱性洗脱液中加酸,由于溶液pH值的变化,发生逆歧化反应而析出泥状粗碘:5NaI+NaIO3+3H2SO4=3I2+3Na2SO4+3H2O氯化钠洗脱液经酸化后再加氧化剂如NaNO2或KClO3溶液,也能使I-离子氧化生成I2
NaNO2使I-离子氧化生