第一章物质结构元素周期表第二节元素周期律(第1课时)学习目标1、理解解核外电子是分层排布的,不同电子层中的电子具有不同的能量
2、掌握核外电子排布的初步规律,并能据此规律画出常见原子的结构示意图
重点核外电子的排布规律,画常见原子的结构示意图
难点核外电子的分层排布
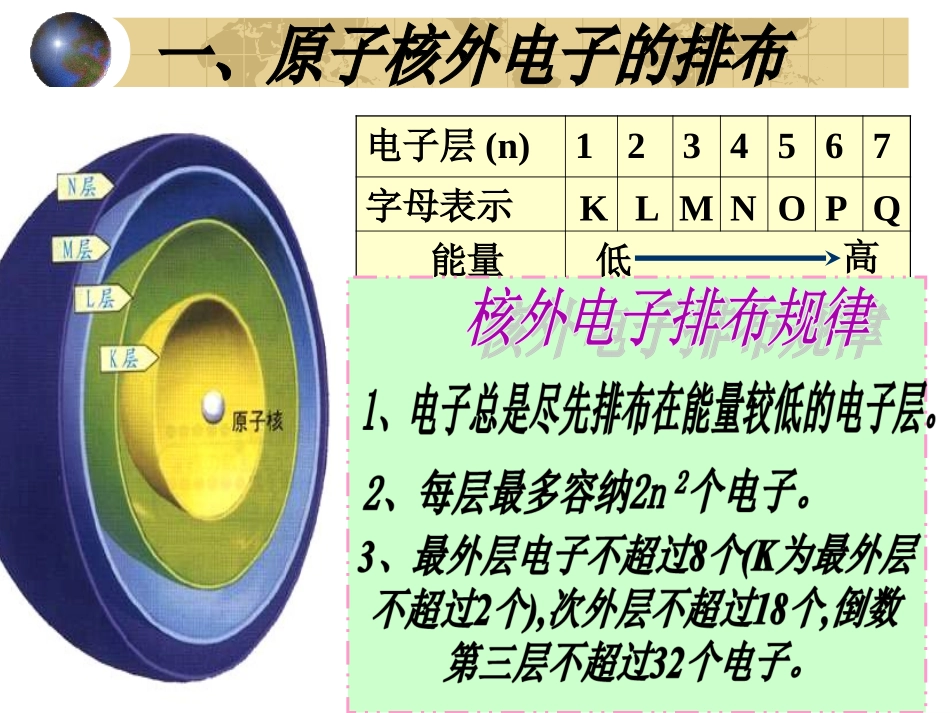
电子层(n)1234567字母表示能量KLMNOPQ低高[练习]1、判断下列示意图是否正确
(A、B、C、D均错)A、B违反了最外层电子数为8的排布规律,C的第一电子层上应为2个电子,D项不符合次外层电子数不超过18的排布规律
根据核外电子排布规律,画出下列元素原子的结构示意图
(1)3Li11Na19K37Rb55Cs(2)9F17Cl35Br53I(3)2He10Ne18Ar36Kr54Xe讨论1、请大家分析稀有气体元素原子电子层排布
稀有气体的最外层电子数有什么特点
[分析]除氦为2个外,其余均为8个
2、元素的化学性质主要决定于哪层电子
稀有气体原名为惰性气体,为什么
[分析]主要决定于最外层电子数
因为它们的化学性质懒惰,不活泼,一般不易和其他物质发学生化学反应
3、我们把以上分析归纳起来,会得出什么结论呢
[分析]原子最外层电子数为8的结构的原子,不易起化学反应
4、元素化学性质主要是什么因素决定的
小结本节课我们重点学习了原子核外电子的排布规律,知道了多电子中的电子排布并不是杂乱无章的,而是遵循一定规律排布的
写出下列离子的离子结构示意图:Mg2+F-Br-Ca2+补充习题1、某元素的原子核外有3个电子层,最外层有4个电子,该原子核内的质子数为()A、14B、15C、16D、172、原子核外的M电子层和L电子层最多容纳的电子数的关系是A、大于B、小于C、等于D不能确定3、C原子L层上的电子数等于次外层上的电子数和电子层数,C是元素
4、若aAn+与bB2-两种离子的核外电子层