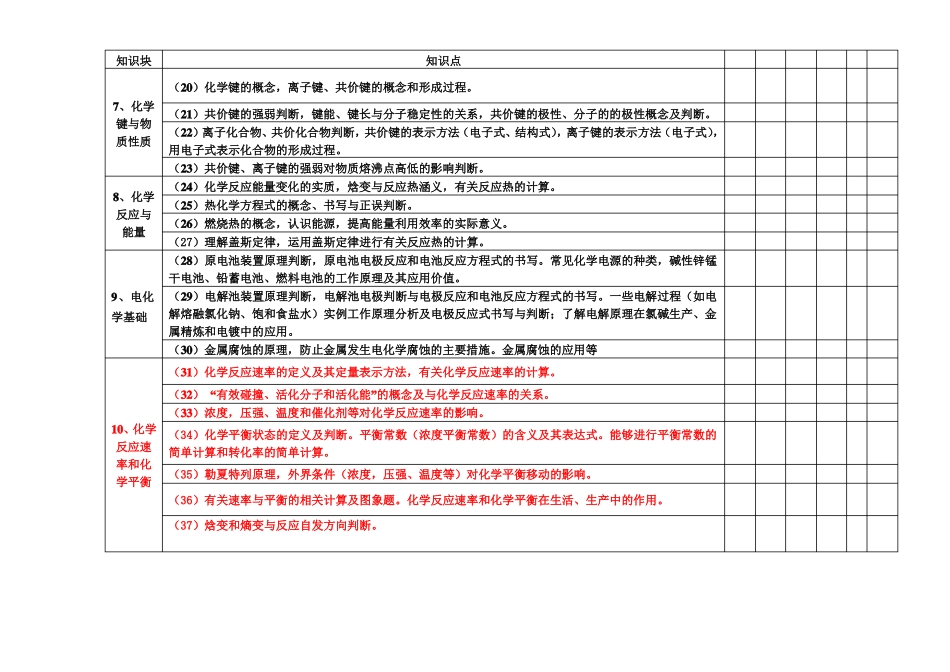
高三化学月考知识点双向细目表知识块1、物质的组成和分类知识点(1)元素与物质的关系
物质的分类方法的应用
(2)物理变化、化学变化的本质,化学反应的基本类型
(3)胶体与溶液、浊液的区别与联系,三种分散系的简单性质(4)物质的量的单位--摩尔(mol),摩尔质量(g•mol-1)、气体摩尔体积(L•mol-1)、物质的量浓度(mol•L-1)、阿伏加德罗常数的含义
2、物质的量(5)物质的量与微粒(原子、分子、离子等)数目、气体体积(标准状况下)、物质的质量之间的相互关系的计算
(6)气态方程公式的应用(相对密度、阿伏加德罗定律、气体相对质量等)
(7)有关物质的量浓度、溶解度、溶质质量分数的简单计算
3、离子反应4、氧化还原反应5、原子结构6、元素周期律与元素性质(8)电解质、非电解质、强电解质和弱电解质的概念判断
(9)离子反应的概念、离子反应发生的条件,离子方程式的书写,离子方程式的正误判断
(10)离子共存判断,常见离子的检验方法
(11)氧化还原反应的本质和特征,氧化还原反应判断,分析氧化还原反应,氧化剂、还原剂判断
(12)常见的氧化剂、还原剂判断,氧化性、还原性强弱的判断
(13)简单氧化还原反应的配平,有关氧化还原反应的计算
(14)原子“三粒子”(质子、中子、电子)的性质、作用和关系
(15)核外电子运动的特点及核外电子分层排布的规律,推断元素种类,原子结构示意图、核外电子排布式和同位素原子表示式
(16)元素、同位素、核素的联系与区别,元素(同位素)相对原子质量的计算
(17)元素周期律的实质及元素周期表的结构(周期、族)(18)元素性质(核外电子排布、原子半径、主要化合价、金属性与非金属性、最高价氧化物水化物的酸碱性、气态氢化物的稳定性)的意义及变化规律(19)同一周期元素性质递变规律与原子结构的关系,同一主族内元素性质递变规律与原子结构的关系