3鲍林规则在对大量的晶体结构进行了仔细的观察、比较和分析并对前人的相关工作进行了深刻总结之后,被誉为20世纪科学怪才的美国科学家鲍林提出了预测离子晶体结构的一些经验规则
鲍林第一规则围绕每一阳离子,形成一个阴离子配位多面体,阴阳离子的间距取决于它们的半径之和,阳离子的配位数则取决于它们的半径之比
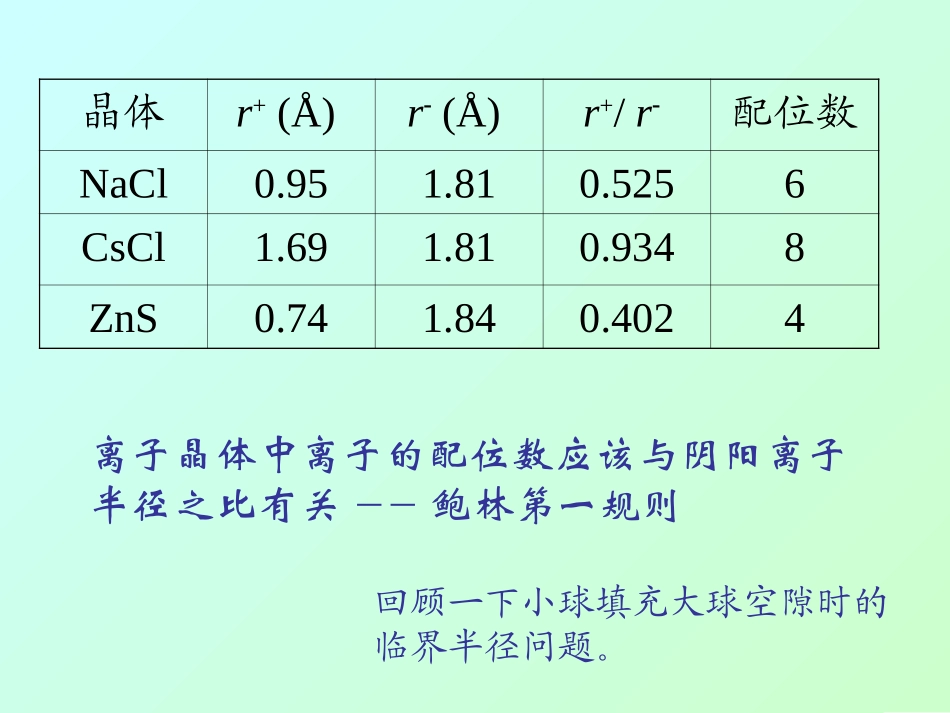
离子晶体中离子的配位数应该与阴阳离子半径之比有关鲍林第一规则晶体r+(Å)r(Å)r+/r配位数NaCl0
5256CsCl1
9348ZnS0
4024回顾一下小球填充大球空隙时的临界半径问题
小球填入大球构成的空隙三角形空隙:r=0
155R四面体空隙:r=0
225R八面体空隙:r=0
414R六面体空隙:r=0
732R关于临界半径比临界半径比决定了离子晶体的结构
但是当阴离子受到阳离子的极化而变形,共价键成分增多以及存在着价键杂化时,这一规则就不适用了
在固体化学发展历史上,离子半径的定义和确定出现了许多版本
在研究晶体结构时,应根据具体情况选择合适的离子半径值
关于离子半径和金属的原子半径一样,结晶学中所指的离子半径也是一个有效半径的概念
严格意义上的离子半径应该是指离子的电子云分布的范围
根据波动力学的计算,离子电子云的分布是无穷的,一个离子的半径也应该是不固定的
离子的有效半径:在离子晶体中一对相邻接触的阴阳离子中心之间的距离就是这两个离子的有效半径之和
关于离子半径阴阳离子中心之间的距离可以借助于X射线衍射分析技术加以准确的测定,但是阴阳离子的分界线在什么地方却难以判断
解决这一困难的方法之一就是对由大量晶体测定的阴阳离子半径和进行比较分析
哥希密德以大量晶体的实验数据为基础推出了氟离子(F)的半径为0
133nm和氧离子(O2)的半径为0
132nm,然后以此为基础从各种离子晶体中