湘潭市一中欢迎您第二章化学物质及其变化第二节离子反应湘潭市一中高一化学备课组复习提问:下列物质哪些是电解质
电解质溶于水后以何种粒子存在
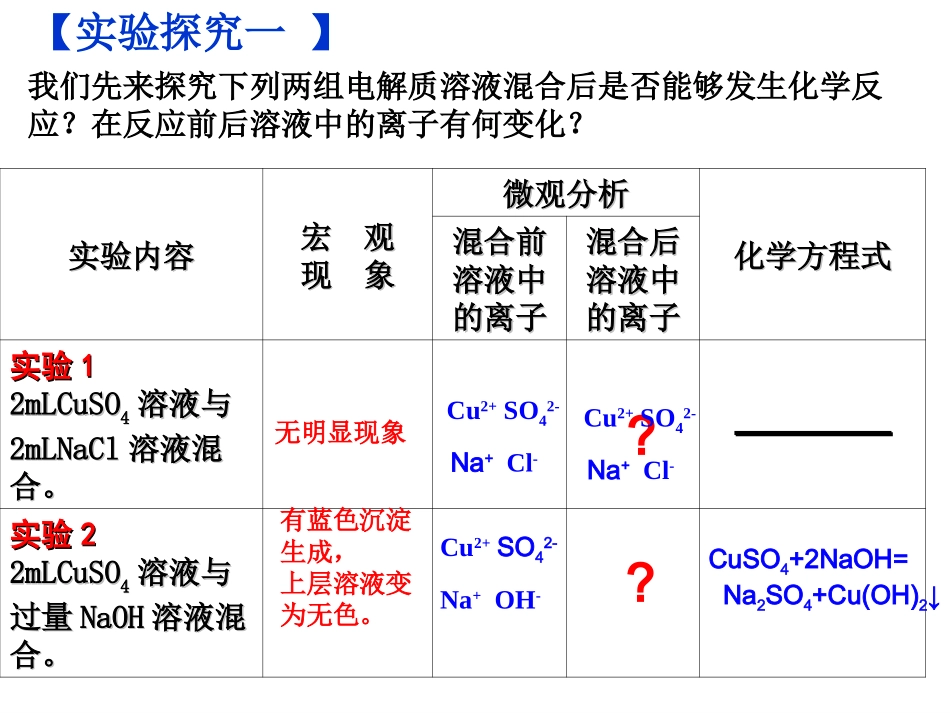
HClNaOHCl2CuSO4FeNa2SO4CO2Na2CO3√√√√√√√√√√√√√√√√√√√√【实验探究一】我们先来探究下列两组电解质溶液混合后是否能够发生化学反应
在反应前后溶液中的离子有何变化
实验内容实验内容宏观宏观现象现象微观分析微观分析化学方程式化学方程式混合前混合前溶液中溶液中的离子的离子混合后混合后溶液中溶液中的离子的离子实验实验112mLCuSO2mLCuSO44溶液与溶液与2mLNaCl2mLNaCl溶液混溶液混合
实验实验222mLCuSO2mLCuSO44溶液与溶液与过量过量NaOHNaOH溶液混溶液混合
无明显现象有蓝色沉淀生成,上层溶液变为无色
Cu2+SO42-Na+Cl-Cu2+SO42-Na+OH-CuSO4+2NaOH=Na2SO4+Cu(OH)2↓
Cu2+SO42-Na+Cl-取反应后的上层清液,滴加BaCl2溶液,若有白色沉淀生成,则溶液中有SO42-,则SO42-没参加反应;反之,则SO42-参加了反应
【实验探究二】请同学们设计实验证明实验2反应后溶液中是否有SO42-
写出使用的试剂、操作过程、实验现象
电解质溶于水电离成为离子,所以电解质在水溶液中发生的反应都是离子反应
有离子参加或生成的反应——离子反应所以,CuSO4溶液与NaOH溶液的反应既是复分解反应又是离子反应1、离子反应1:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4+SO42-2:Cu2++2OH-=Cu(OH)2↓↙↘↙↘↙↘Cu2++SO42-+2Na++2OH-=Cu(OH)2↓↓【讨论分析】CuSO4和NaOH反应过程中离子的种类和数目的变化
思考:上面这个式子是不是我们以前学过的化学方程