第二节水的电离与溶液的酸碱性[问题讨论][问题讨论]----------水能电离吗
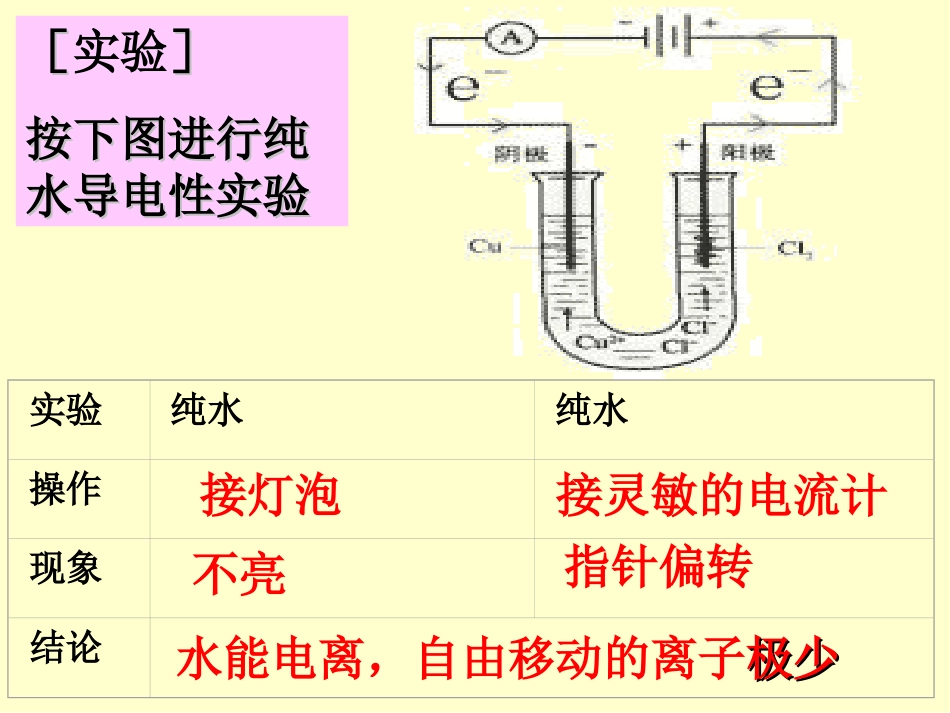
[[实验]]按下图进行纯按下图进行纯水导电性实验水导电性实验实验纯水纯水操作现象结论接灯泡接灵敏的电流计不亮指针偏转水能电离,自由移动的离子极少极少一、水的电离一、水的电离1
水是一种极弱的电解质-------能发生微弱的电离
电离产生等量的H+离子和OHˉ离子22水的电离方程式水的电离方程式H2O+H2OH3O++OHˉH△>0水合氢离子简写为:H2OH++OHˉH△>0水达到电离平衡时有:K(µçÀë)C(H2O)C(OH-)C(H+)=C(H+)·C(OH-)=K(电离)·C(H2O)将C(H2O)看作一个常数所以:C(H+)·C(OH-)=Kw(常数)水的离子积常数(1)定义---------一定温度下,水溶液中氢离子浓度[C(H+)]与氢氧根离子浓度[C(OH-)]的乘积为一常数,把这一常数叫做水的离子积常数,简称为水的离子积
用符号Kw表示3水的离子积常数Kw即:Kw=C(H+)·C(OH-)=常数Kw的变形式有:Kw=C(H+)C(OH-)Kw=C(H+)C(OH-)[注意]a25(℃常温)下的纯水纯水:C(H+)=C(OH-)=1×10-7mol/LKw=C(H+)·C(OH-)=1×10-7mol/L×1×10-7mol/L=1×10-14(mol/L)2即:25℃时Kw=1×10-14(mol/L)2b100(℃常温)下的纯水纯水:[讨论]-------25℃时,酸、碱、盐的水溶液的Kw仍然为1×10-14(mol/L)2
是C(H+)=C(OH-)=1×10-6mol/LKw=C(H+)·C(OH-)=1×10-6mol/L×1×10-6mol/L=1×10-12(mol/L)2d在不同溶液中,C(H+)和C(OH-)不一不一定相