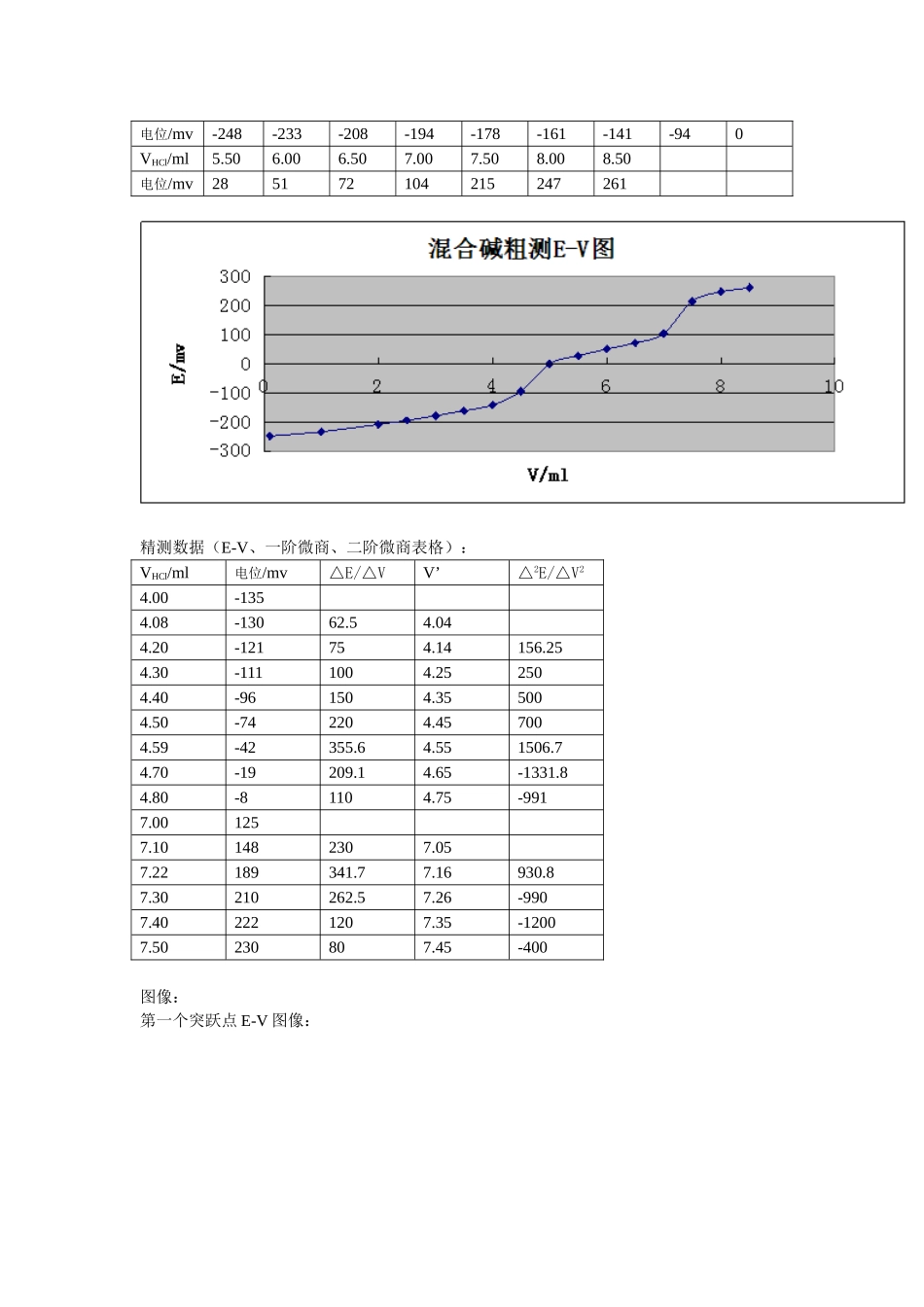
电位滴定法对混合碱的测定实验目的:了解HCl滴定混合碱的原理、突跃曲线和方法;掌握ZD-2型自动电位滴定仪(pH计)的使用;利用仪器和已知浓度盐酸测定混合碱的组成;掌握电位滴定法分析的操作
实验结果:两次滴定突跃对应的消耗的HCl体积V1=4
55ml和V2=2
62ml;混合碱组成是NaOH和Na2CO3;两者的含量分别为CNaOH=0
0193mol/L,CNa2CO3=0
0262mol/L,即混合碱中NaOH和Na2CO3质量分数分别为:21
75%和78
实验背景:混合碱是指碳酸钠、碳酸氢钠和氢氧化钠三种碱的不同组成的总称,其混合的形式可能为:(1)Na2CO3+NaHCO3(2)Na2CO3+NaOH(3)Na2CO3含量检测可采用双指示剂法,用HCl标液滴定混合碱时有两个化学计量点:第一个计量点时,反应可能为:Na2CO3+HCl==NaHCO3+NaClNaOH+HCl==NaCl+H2O溶液的pH值为8
31,用酚酞为指示剂(变色范围8
0),从红色变为几乎无色时为终点,滴定体积为V1(ml)
第二个化学计量点时,滴定反应为:NaHCO3+HCl==NaCl+CO2↑+H2O溶液pH为3
9,以二甲基黄-溴甲酚绿为指示剂,终点呈亮黄色,或者甲基橙做指示剂,滴定体积为V2(ml)
当V2>V1时,则混合碱为Na2CO3+NaHCO3;当V1>V2时,为Na2CO3+NaOH;当V1=V2时,为Na2CO3
实验原理:本实验不同于双指示剂法,而是利用滴定过程中随着酸的加入和反应的进行,溶液pH发生变化,导致溶液的电位变化,通过H+电极和甘汞电极组成的pH计来测定电位,并指示反应进行的程度和速率
电位滴定法:进行电位滴定时,甘汞电极作参比电极,H+电极作指示电极,组成工作电池
随着滴定剂的加入,由于发生化学反应,被测离子浓度不断变化,指示电极的