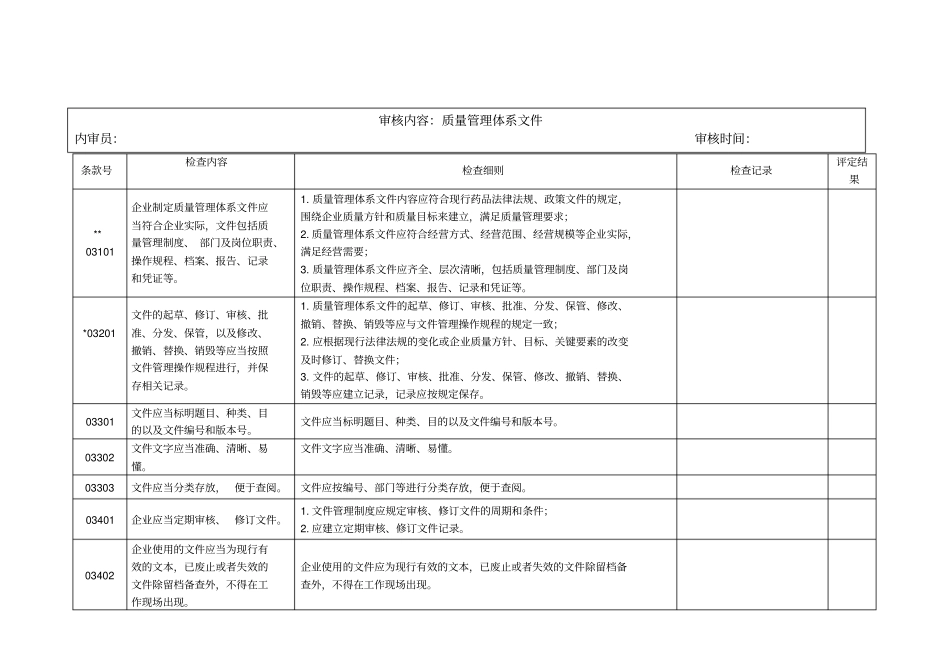
条款号检查内容检查细则检查记录评定结果**03101企业制定质量管理体系文件应当符合企业实际,文件包括质量管理制度、部门及岗位职责、操作规程、档案、报告、记录和凭证等
质量管理体系文件内容应符合现行药品法律法规、政策文件的规定,围绕企业质量方针和质量目标来建立,满足质量管理要求;2
质量管理体系文件应符合经营方式、经营范围、经营规模等企业实际,满足经营需要;3
质量管理体系文件应齐全、层次清晰,包括质量管理制度、部门及岗位职责、操作规程、档案、报告、记录和凭证等
*03201文件的起草、修订、审核、批准、分发、保管,以及修改、撤销、替换、销毁等应当按照文件管理操作规程进行,并保存相关记录
质量管理体系文件的起草、修订、审核、批准、分发、保管、修改、撤销、替换、销毁等应与文件管理操作规程的规定一致;2
应根据现行法律法规的变化或企业质量方针、目标、关键要素的改变及时修订、替换文件;3
文件的起草、修订、审核、批准、分发、保管、修改、撤销、替换、销毁等应建立记录,记录应按规定保存
03301文件应当标明题目、种类、目的以及文件编号和版本号
文件应当标明题目、种类、目的以及文件编号和版本号
03302文件文字应当准确、清晰、易懂
文件文字应当准确、清晰、易懂
03303文件应当分类存放,便于查阅
文件应按编号、部门等进行分类存放,便于查阅
03401企业应当定期审核、修订文件
文件管理制度应规定审核、修订文件的周期和条件;2
应建立定期审核、修订文件记录
03402企业使用的文件应当为现行有效的文本,已废止或者失效的文件除留档备查外,不得在工作现场出现
企业使用的文件应为现行有效的文本,已废止或者失效的文件除留档备查外,不得在工作现场出现
审核内容:质量管理体系文件内审员:审核时间:03501企业应当保证各岗位获得与其工作内容相对应的必要文件,并严格按照规定开展工作