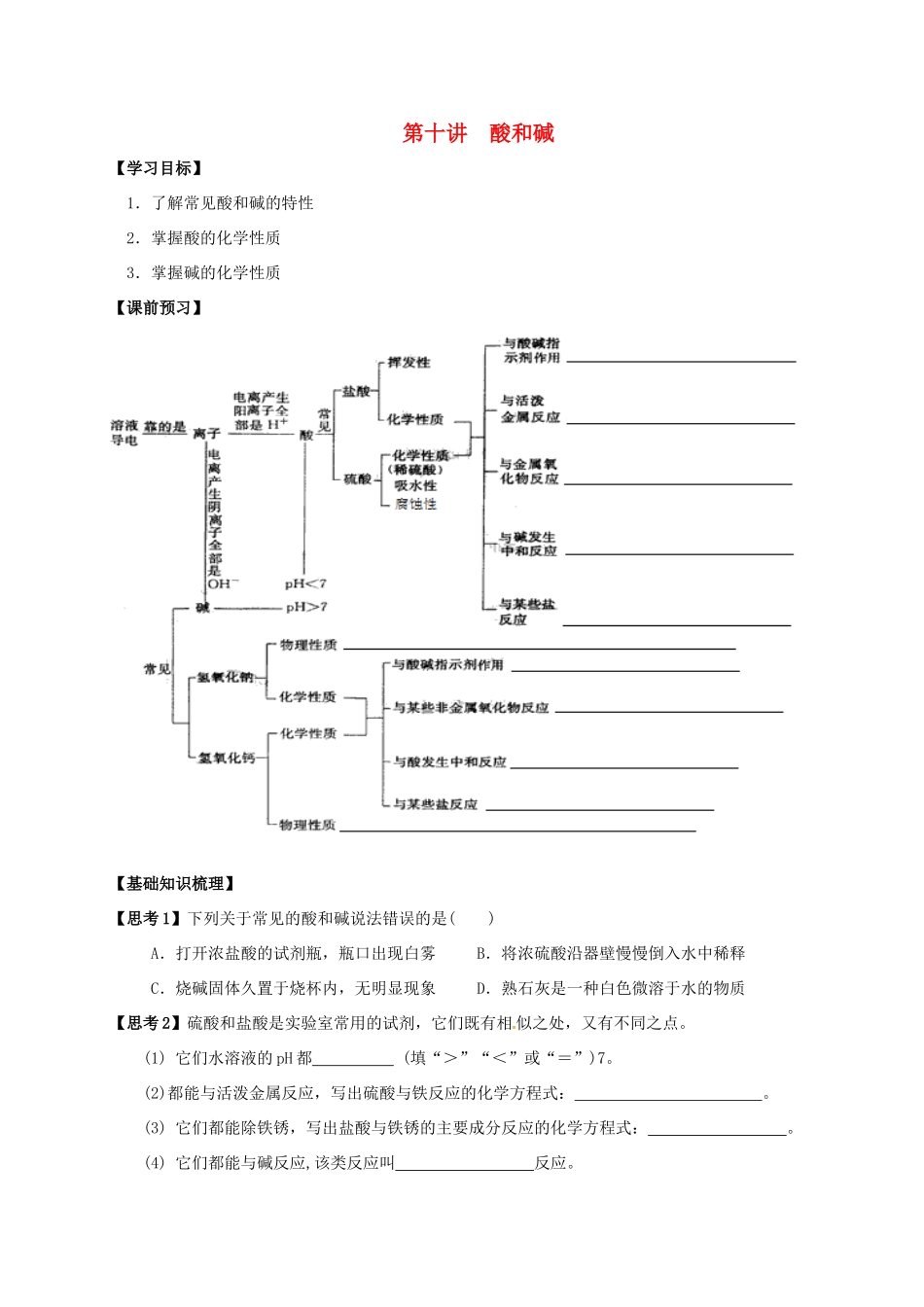
第十讲酸和碱【学习目标】1.了解常见酸和碱的特性2.掌握酸的化学性质3.掌握碱的化学性质【课前预习】【基础知识梳理】【思考1】下列关于常见的酸和碱说法错误的是()A.打开浓盐酸的试剂瓶,瓶口出现白雾B.将浓硫酸沿器壁慢慢倒入水中稀释C.烧碱固体久置于烧杯内,无明显现象D.熟石灰是一种白色微溶于水的物质【思考2】硫酸和盐酸是实验室常用的试剂,它们既有相似之处,又有不同之点
(1)它们水溶液的pH都(填“>”“<”或“=”)7
(2)都能与活泼金属反应,写出硫酸与铁反应的化学方程式:
(3)它们都能除铁锈,写出盐酸与铁锈的主要成分反应的化学方程式:
(4)它们都能与碱反应,该类反应叫反应
(5)写出把硫酸转化为盐酸的化学方程式:
【思考3】根据学习碱的化学性质,完成下列问题
(1)碱溶液能使无色酚酞溶液变
(2)氢氧化钠暴露在空气中变质的化学方程式为,所以氢氧化钠必须保存
(3)向烧杯中的硫酸铜溶液中滴加氢氧化钠溶液,反应的现象是
(4)碱溶液有相似的化学性质,是因为碱溶液中都含有
【典型问题分析】例1:如图是物质之间发生化学反应的颜色变化
(1)请你在编号②、③处各填入一种物质,②是;③是;(2)根据上图总结出稀硫酸的五个化学性质,请写出编号①稀硫酸的化学性质;(3)若编号④的物质是碱,请你写出符合编号④的一个化学方程式:
例2:为验证CO2与NaOH能够发生反应,某同学按图组装实验装置,并进行实验
(1)观察到的现象是“气球先膨胀,后变瘪”,则加入试剂的顺序应该是
A.先加盐酸,再加氢氧化钠溶液B.先加氢氧化钠溶液,再加盐酸(2)请解释气球“先膨胀”的原因:_____________________________________________
(3)写出气球“后变瘪”的化学方程式:_____________________________________________