课题三氧气的实验室制取加热固体+固体气体试管口略向下倾斜(10~150角)加热法制取氧气的发生装置:1
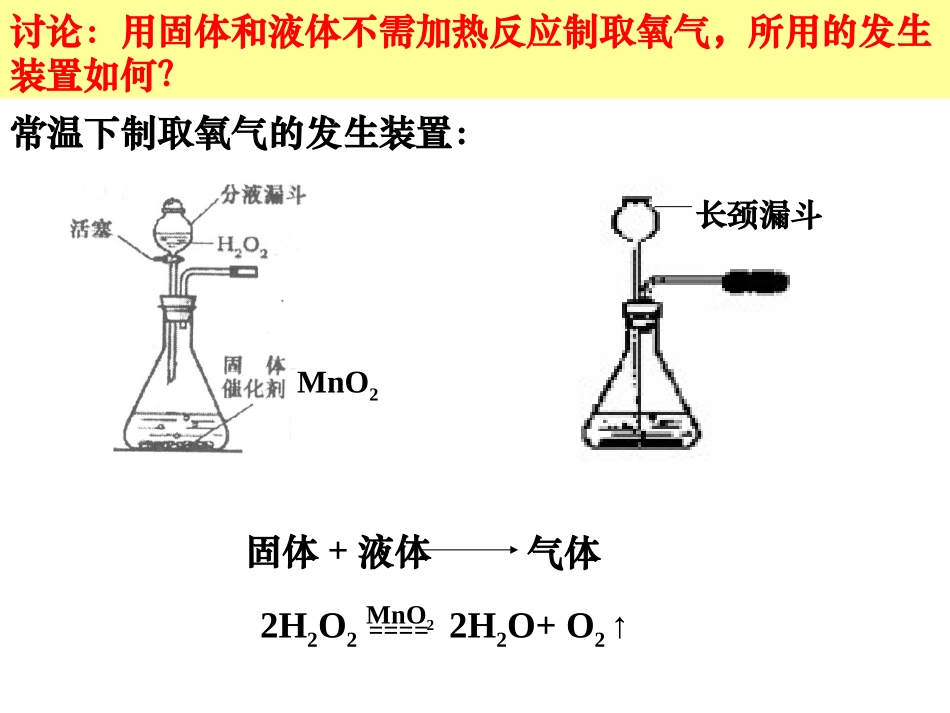
气体发生装置(由反应物的状态及反应条件决定)仪器装置(发生装置、收集装置)固体+液体气体常温下制取氧气的发生装置:讨论:用固体和液体不需加热反应制取氧气,所用的发生装置如何
2H2O22H2O+O2↑====MnO2MnO2长颈漏斗2
收集装置和收集方法向上排空气法排水法(较纯)氧气的密度比空气略大氧气不易溶于水,不与水发生反应(由氧气的密度和溶解性决定)集气瓶玻璃片向上排空气法(较干燥)导管导管水槽集气瓶排水法(较纯)实验装置的连接原则:从左到右,由下而上
注意:加热高锰酸钾时,试管口要塞一团棉花,防止高锰酸钾进入导管;加热氯酸钾时,试管口不能塞棉花
试管导管酒精灯铁架台水槽集气瓶棉花用加热法制取氧气的整套装置:固体+液体气体常温下制取氧气的整套装置:2H2O22H2O+O2↑====MnO2一、实验室制取氧气(一)实验室制取氧气的反应原理:过氧化氢溶液H2O2(无色)高锰酸钾KMnO4(暗紫色或者紫黑色)氯酸钾KClO3(白色)二氧化锰MnO2(黑色)实验药品及其颜色1、分解过氧化氢(H2O2)与二氧化锰(MnO2黑色)的混合物制氧气:原理用化学方程式表示为:2H2O2==2H2O+O2↑(1)(2)现象:⑴⑵有少量气泡,木条不复燃有大量气泡,木条复燃说明:H2O2在常温下反应速度较慢,产生少量氧气
说明:MnO2加快了H2O2反应产生氧气的速度
即:在这个反应中,MnO2是催化剂,只起催化作用,而MnO2本身的质量和化学性质均不改变
催化剂(触媒):化学反应里能改变其他物质的化学反应速率,本身的质量和化学性质在反应前后都不变的物质
催化剂及其催化作用:加快或者减慢c
注意几点:(1)催化剂只改变反应速度,不能使生成物质量增加
(2)催化剂不影响反应的进行