溶质的质量分数溶剂:能溶解其他物质的物质叫做溶剂
回顾复习溶质:被溶解的物质叫做溶质
饱和溶液:在一定温度下,向一定量溶剂里加入某种溶质,当溶质不能继续溶解时,所得到的溶液叫做饱和溶液
溶解度:表示在一定温度下,某固态物质在100g溶剂里达到饱和状态时所溶解的质量
1、什么叫溶剂
2、什么叫溶质
3、什么叫饱和溶液
4、什么叫溶解度
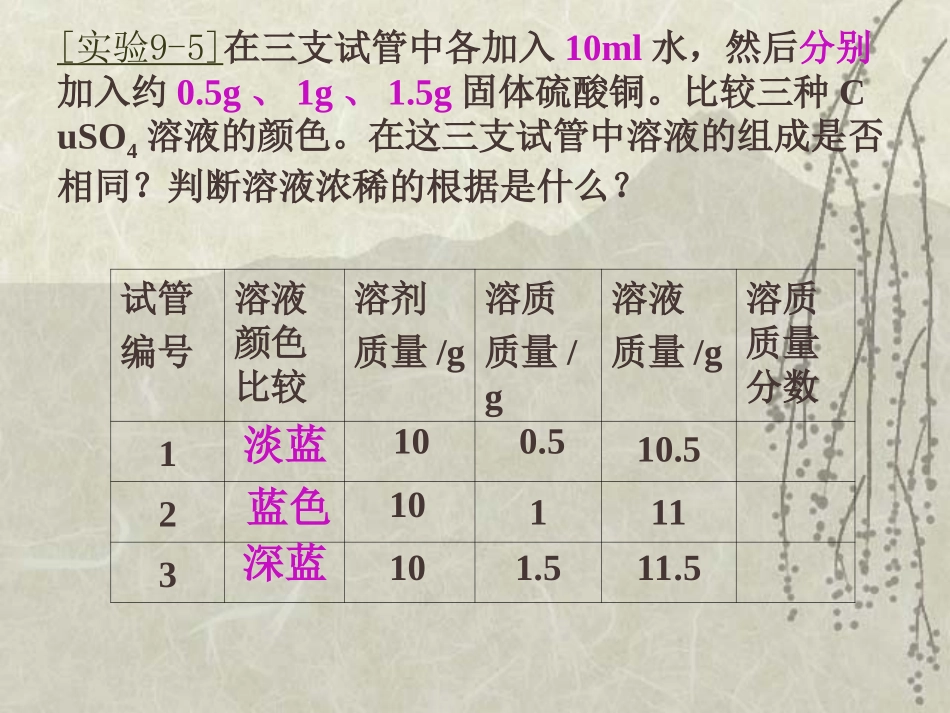
[实验9-5]在三支试管中各加入10ml水,然后分别加入约0
5g、1g、1
5g固体硫酸铜
比较三种CuSO4溶液的颜色
在这三支试管中溶液的组成是否相同
判断溶液浓稀的根据是什么
试管编号溶液颜色比较溶剂质量/g溶质质量/g溶液质量/g溶质质量分数1231010100
5淡蓝蓝色深蓝对于有色溶液来说,根据颜色的深浅可以区分溶液是浓还是稀
但是这种方法比较粗略,不能准确地表明一定量的溶液里究竟含有多少溶质
在实际应用中,常常要准确知道一定量溶液时含有溶质的质量
如在施用农药时、生产医用生理盐水和葡萄糖时等等
因此,我们需要准确知道溶液的组成
那用什么方法可以表示溶液的组成呢
溶质的质量分数溶质的质量分数:溶质质量与溶液质量之比
溶质的质量分数=×100%溶质质量溶液质量=×100%溶质质量溶质质量+溶剂质量溶质质量/g溶剂质量/g溶液质量/g溶质质量分数101009610015016%35
7100请利用所学的溶质质量分数公式填空9010%44%24126135
3%图示:是病人输液时用的一瓶葡萄糖注射液标签,请你根据标签给出的数据计算该溶液中含水g
葡萄糖注射液GluCoseinjection规格:250ml内含葡萄糖:12
5g5%生产批号:020222032有效期:至2008年7月237
5例、已知20℃时食盐的溶解度为36g,求20℃时食盐饱和溶液的溶质质量分数
解:20℃时食盐饱和溶液的溶质质量分