黄冈中学初三化学实验室制取氧气1、反应原理①加热氯酸钾制取氧气:氯酸钾氯化钾+氧气
②加热高锰酸钾制取氧气:高锰酸钾锰酸钾+二氧化锰+氧气③分解过氧化氢制取氧气:过氧化氢水+氧气
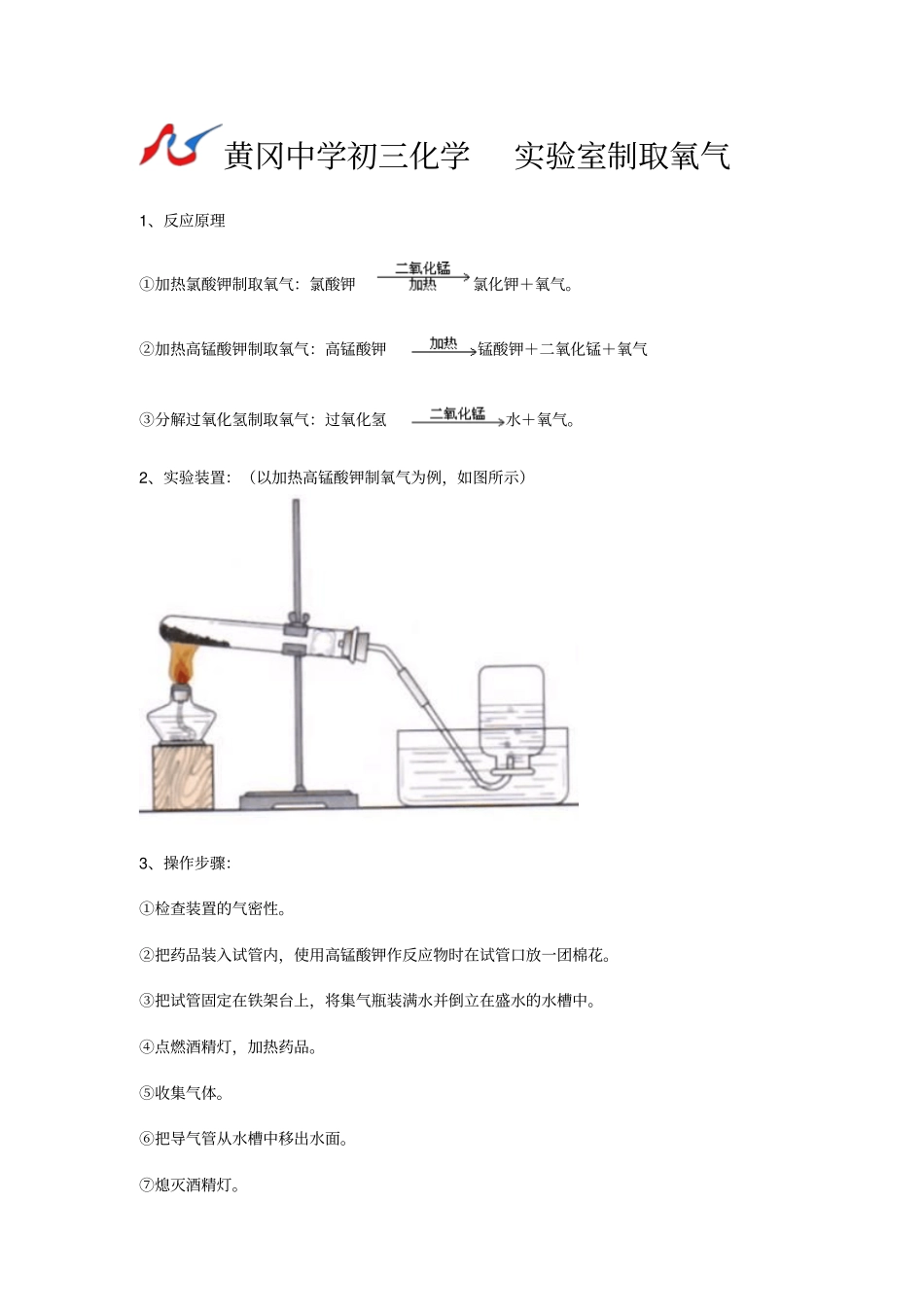
2、实验装置:(以加热高锰酸钾制氧气为例,如图所示)3、操作步骤:①检查装置的气密性
②把药品装入试管内,使用高锰酸钾作反应物时在试管口放一团棉花
③把试管固定在铁架台上,将集气瓶装满水并倒立在盛水的水槽中
④点燃酒精灯,加热药品
⑥把导气管从水槽中移出水面
⑦熄灭酒精灯
4、收集方法:①排水集气法(因为氧气不易溶于水)
操作要点:把盛满水的集气瓶(无泡)倒立在水中,排水充气,取出放置
②向上排空气法(因为氧气的密度略大于空气)
操作要点:使导气管尽量伸入集气瓶底便于排尽空气
5、检验:将带火星的木条伸入集气瓶内,若木条复燃,证明瓶内气体是氧气
氧气可以使带火星的木条复燃6、验满:若用向上排空气法收集氧气,验满时,取一根带火星的木条,放在集气瓶口,若木条复燃,则证明氧气已集满
7、放置:因为氧气的密度大于空气的密度,故应正放在桌面上
8、注意事项:①在用氯酸钾或高锰酸钾制取氧气时,试管口应略向下倾斜,原因是防止加热时药品中的湿存水倒流炸裂试管
②铁夹应夹在距试管口1/3处,原因是利于加热
③导管伸入试管内要刚露出橡皮塞,原因是利于排出产生的气体
④用排水法收集氧气时,不宜立即收集,待有连续均匀的气泡产生时再收集,原因是开始的气泡是试管内的空气,若立即收集则氧气不纯
⑤排气法收集气体时,导管要伸入接近集气瓶底部,原因是利于充分排出瓶内空气
⑥实验结束时,先将导管移出水面,再熄灭酒精灯,原因是防止水槽中的水倒吸炸裂试管
⑦如果用高锰酸钾制氧气时,试管口应塞一小团棉花,原因是防止高锰酸钾粉末进入导管
(二)、正确选用气体的收集方法原则:易溶于水的气体选排空气法收集,根据气体的密度定“向上”或