化学史话在1774年,瑞典化学家舍勒(ScheeleKW,1742-1786)在从事软锰矿的研究时发现:软锰矿与盐酸混合后加热就会生成一种令人窒息的黄绿色气体,这种气体微溶于水,使水显酸性
能漂白有色花朵和绿叶,还能和各种金属发生反应
当时,大化学家拉瓦锡认为氧是酸性的起源,一切酸中都含有氧
舍勒及许多化学家都坚信拉瓦锡的观点,认为这种黄绿色的气体是一种化合物,是由氧和另外一种未知的基所组成的,所以舍勒称它为“氧化盐酸”
但英国化学家戴维(DavySH,1778-1829)却持有不同的观点,他想尽了一切办法也不能从氧化盐酸中把氧夺取出来,他怀疑氧化盐酸中根本就没有氧存在
1810年,戴维以无可辩驳的事实证明了所谓的氧化盐酸不是一种化合物,而是一种化学元素的单质
他将这种元素命名为“Chlorine”
它的希腊文原意是“绿色”
中文译名为氯
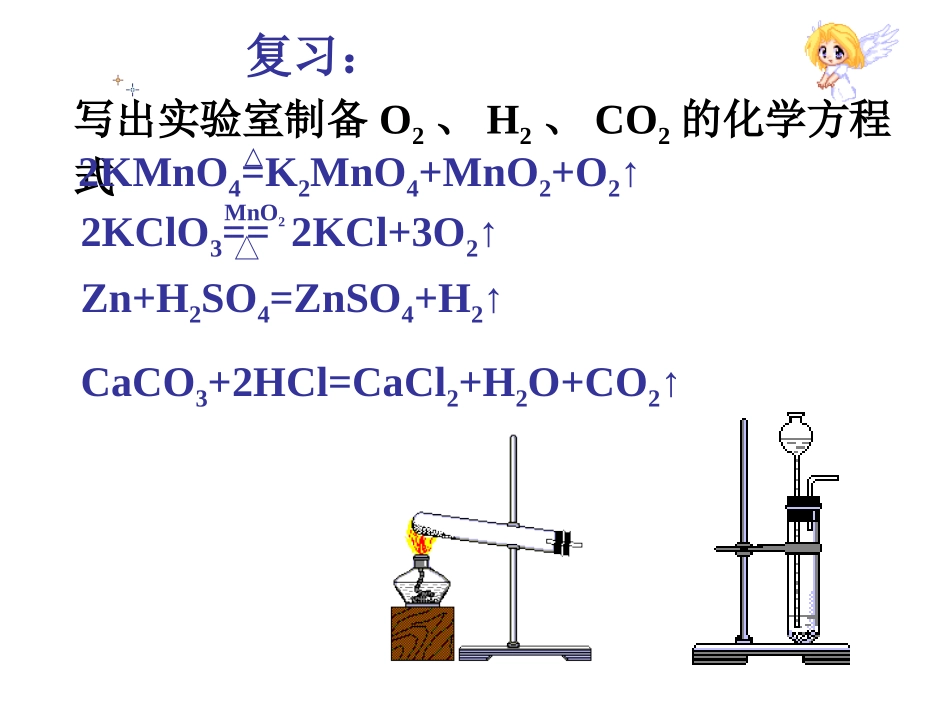
2KClO3==2KCl+3O2↑MnO2写出实验室制备O2、H2、CO2的化学方程式复习:Zn+H2SO4=ZnSO4+H2↑CaCO3+2HCl=CaCl2+H2O+CO2↑2KMnO4=K2MnO4+MnO2+O2↑△气体发生装置是根据反应物的状态和反应的条件确定的,收集方法是跟据气体的物理性质确定的
思考:氯气有何物理性质
黄绿色气体有刺激性气味密度比空气大可溶于水实验室氯气是如何制备的呢
1、反应原理:用氧化剂在适当的条件下将负一价氯氧化成为零价氯
2、药品:MnO2和浓盐酸3、化学方程式:离子方程式:得2e-失2×e-二、氯气的实验室制法+4-1+2-10MnO2+4H++2Cl-=Mn2++2H2O+Cl2↑△固液反应,需加热反应物的状态和反应的条件:电子转移
MnO2+4HCl(浓)=MnCl2+2H2O+Cl2↑△4、气体发生装置与仪器分液漏斗圆底烧瓶酒精灯铁架台(带铁圈铁夹)石棉网导管思考此装置与制H2的装置有何不同