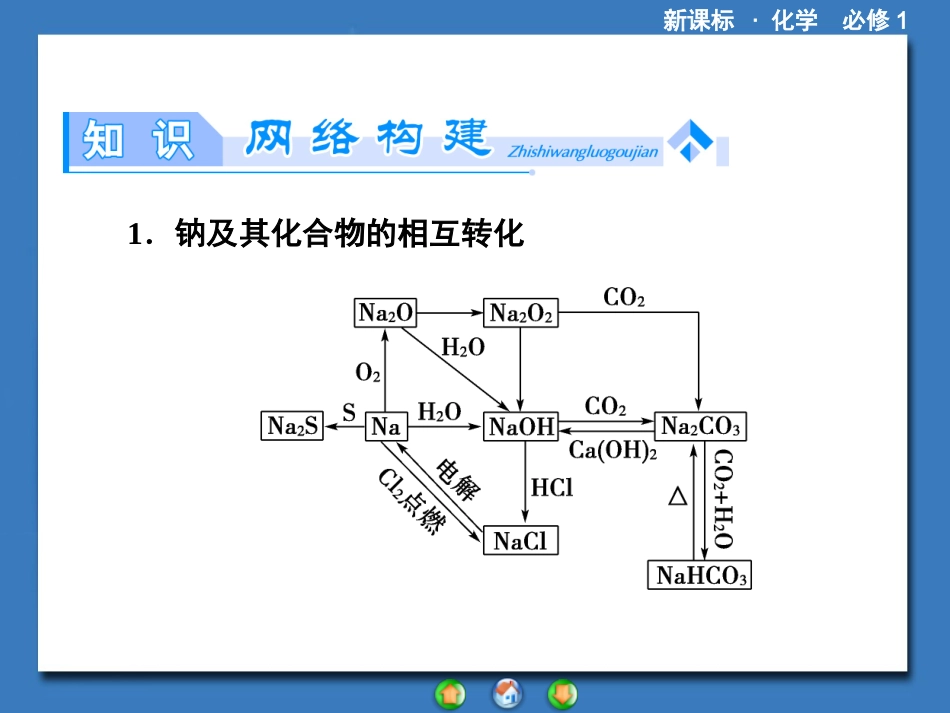
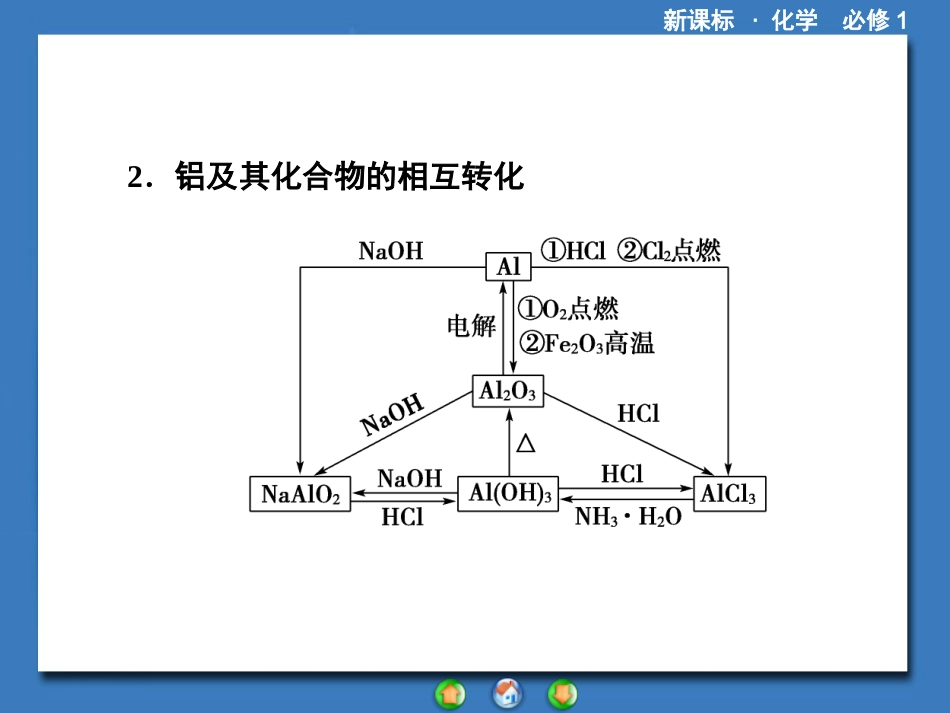
新课标·化学必修1新课标·化学必修11.钠及其化合物的相互转化新课标·化学必修12.铝及其化合物的相互转化新课标·化学必修13.铁及其化合物的相互转化新课标·化学必修11
关系式法当已知量和未知量之间是靠多个反应来联系时,只需直接确定已知量和未知量之间的比例关系,即“关系式”
(1)根据化学方程式确定关系式写出发生反应的化学方程式,根据量的关系写出关系式
新课标·化学必修1例如:把CO还原Fe2O3生成的CO2通入到澄清的石灰水中,求生成沉淀的量
发生反应的化学方程式:3CO+Fe2O3=====△2Fe+3CO2CO2+Ca(OH)2===CaCO3↓+H2O则关系式为3CO~3CO2~3CaCO3,即CO~CaCO3
(2)根据原子守恒确定关系式上述例子中也可直接根据碳原子守恒得出CO~CaCO3
新课标·化学必修12.守恒法守恒关系特征质量守恒宏观:反应前后物质的质量守恒微观:反应前后元素的原子个数守恒电子守恒氧化还原反应中,得失电子守恒电荷守恒电解质溶液中,阳离子所带的正电荷总数等于阴离子所带的负电荷总数离子方程式中,反应物所带的电荷总数等于生成物所带的电荷总数,且电性相同新课标·化学必修13
差量法根据化学反应前后物质的有关物理量发生的变化,找出“理论差量”,如反应前后的质量差、物质的量差、气体体积差等
该差量的大小与反应物的有关量成正比
差量法就是借助这种比例关系,解决一定量变的计算题的方法
例如,把一铁棒插入CuSO4溶液后,过一段时间取出,铁棒质量增加了4g,据此可求出参加反应的Fe的质量
新课标·化学必修1Na2CO3、NaHCO3的混合物与100mL3mol/L盐酸恰好完全反应,产生4
48L(标准状况)能使澄清石灰水变浑浊的气体,请计算混合物中Na2CO3的物质的量
【解析】新课标·化学必修1设Na2CO3的物质的量为x,NaHCO3的物质的量为y