第1课时物质的分离与提纯[学习目标]掌握结晶、蒸馏、萃取、分液、过滤等分离提纯混合物方法的原理、所需仪器、基本操作、注意事项,能够灵活地选用合适的方法分离、提纯混合物
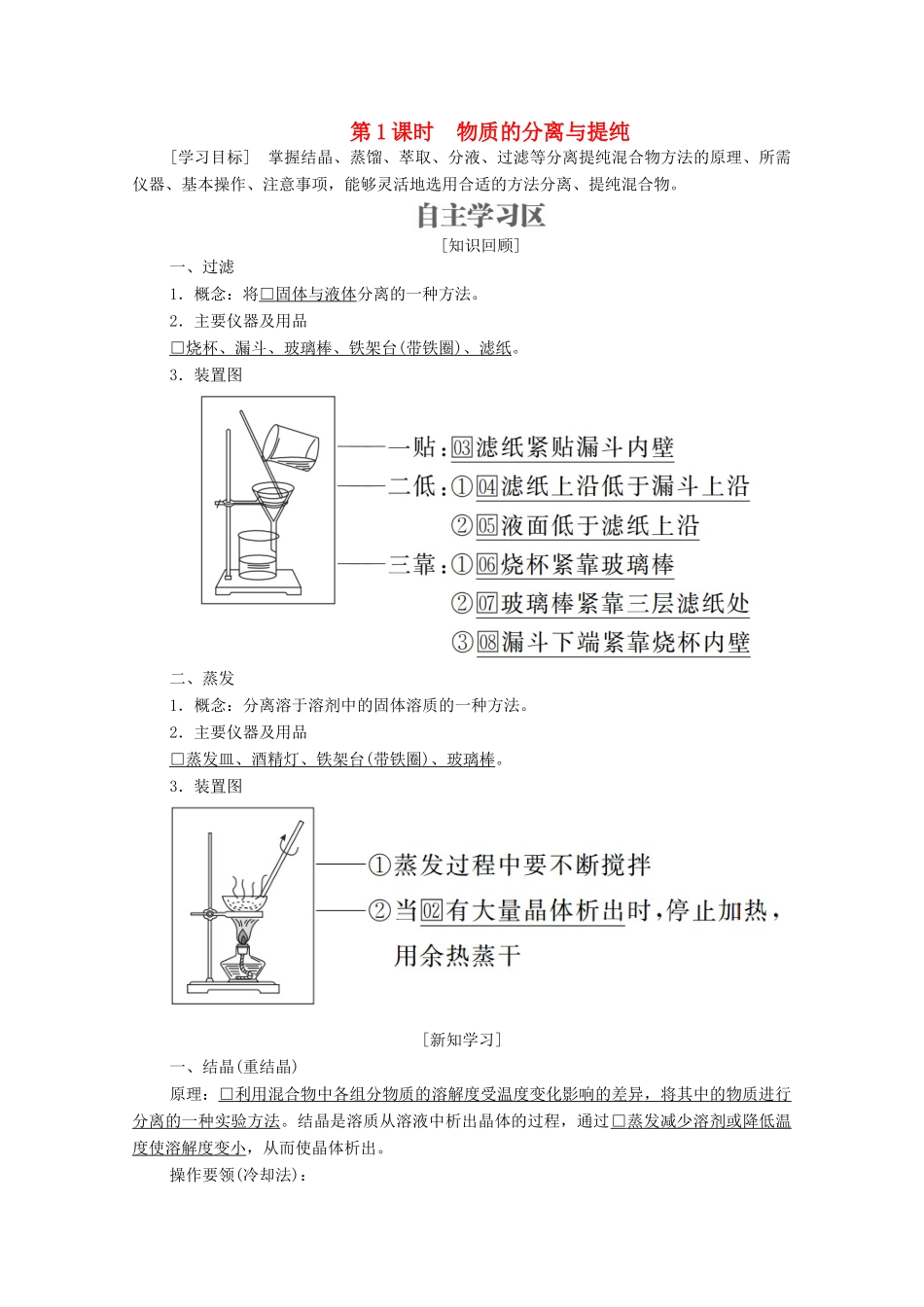
[知识回顾]一、过滤1.概念:将□固体与液体分离的一种方法
2.主要仪器及用品□烧杯、漏斗、玻璃棒、铁架台(带铁圈)、滤纸
3.装置图二、蒸发1.概念:分离溶于溶剂中的固体溶质的一种方法
2.主要仪器及用品□蒸发皿、酒精灯、铁架台(带铁圈)、玻璃棒
3.装置图[新知学习]一、结晶(重结晶)原理:□利用混合物中各组分物质的溶解度受温度变化影响的差异,将其中的物质进行分离的一种实验方法
结晶是溶质从溶液中析出晶体的过程,通过□蒸发减少溶剂或降低温度使溶解度变小,从而使晶体析出
操作要领(冷却法):通常先在较高温度下溶解固体并形成浓溶液,然后降低温度,溶解度受温度变化影响较大的溶质析出晶体
【注意】重结晶又叫再结晶,即让晶体重新溶解,再进行蒸发或降温冷却,让晶体重复结晶、过滤,以达到更进一步分离或提纯混合物的目的
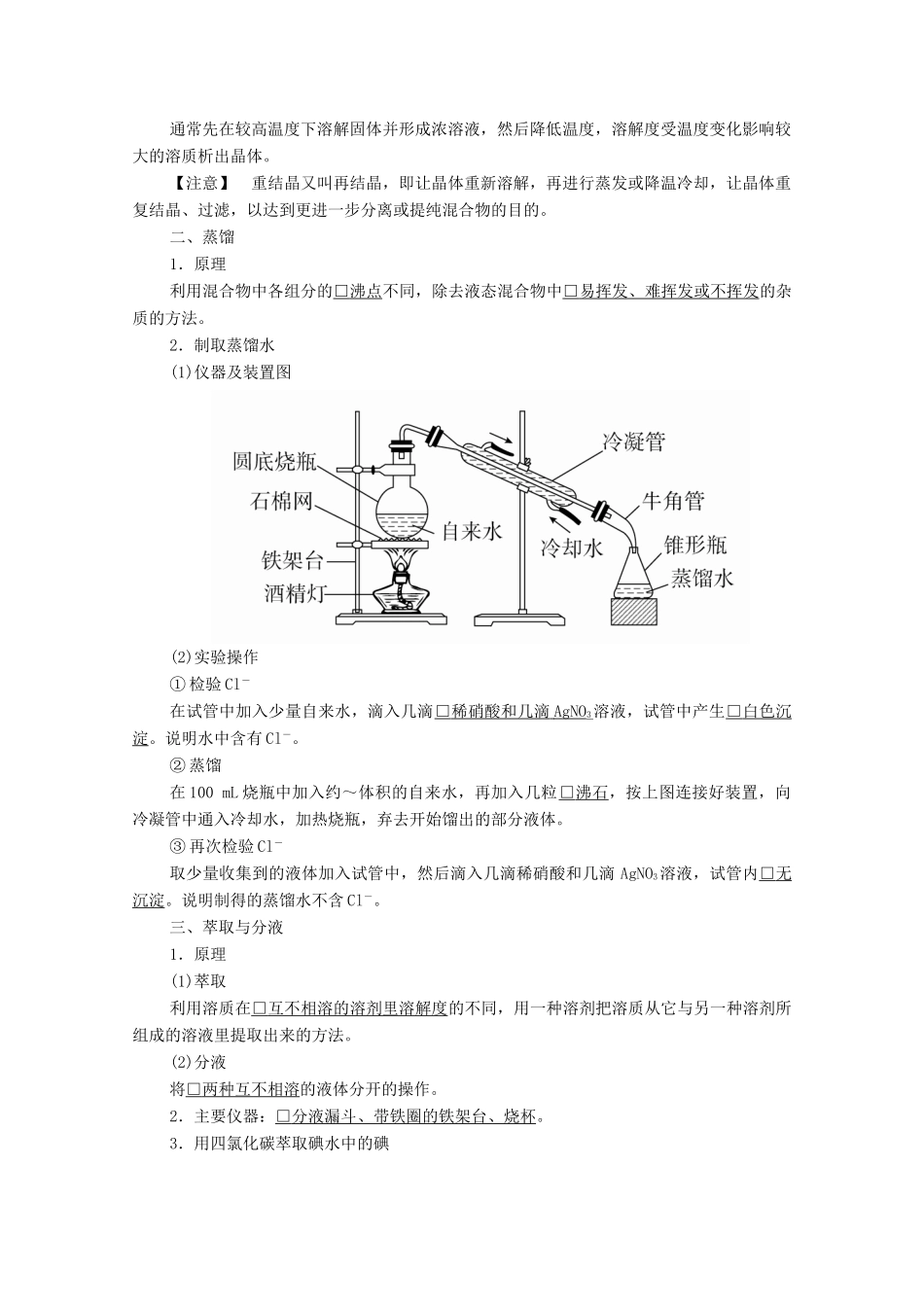
二、蒸馏1.原理利用混合物中各组分的□沸点不同,除去液态混合物中□易挥发、难挥发或不挥发的杂质的方法
2.制取蒸馏水(1)仪器及装置图(2)实验操作①检验Cl-在试管中加入少量自来水,滴入几滴□稀硝酸和几滴AgNO3溶液,试管中产生□白色沉淀
说明水中含有Cl-
②蒸馏在100mL烧瓶中加入约~体积的自来水,再加入几粒□沸石,按上图连接好装置,向冷凝管中通入冷却水,加热烧瓶,弃去开始馏出的部分液体
③再次检验Cl-取少量收集到的液体加入试管中,然后滴入几滴稀硝酸和几滴AgNO3溶液,试管内□无沉淀
说明制得的蒸馏水不含Cl-
三、萃取与分液1.原理(1)萃取利用溶质在□互不相溶的溶剂里溶解度的不同,用一种溶剂把溶质从它与另一种溶剂所组成的溶液里提取出来的方法
(2)分液将□两种互不相溶的液体分开的操作