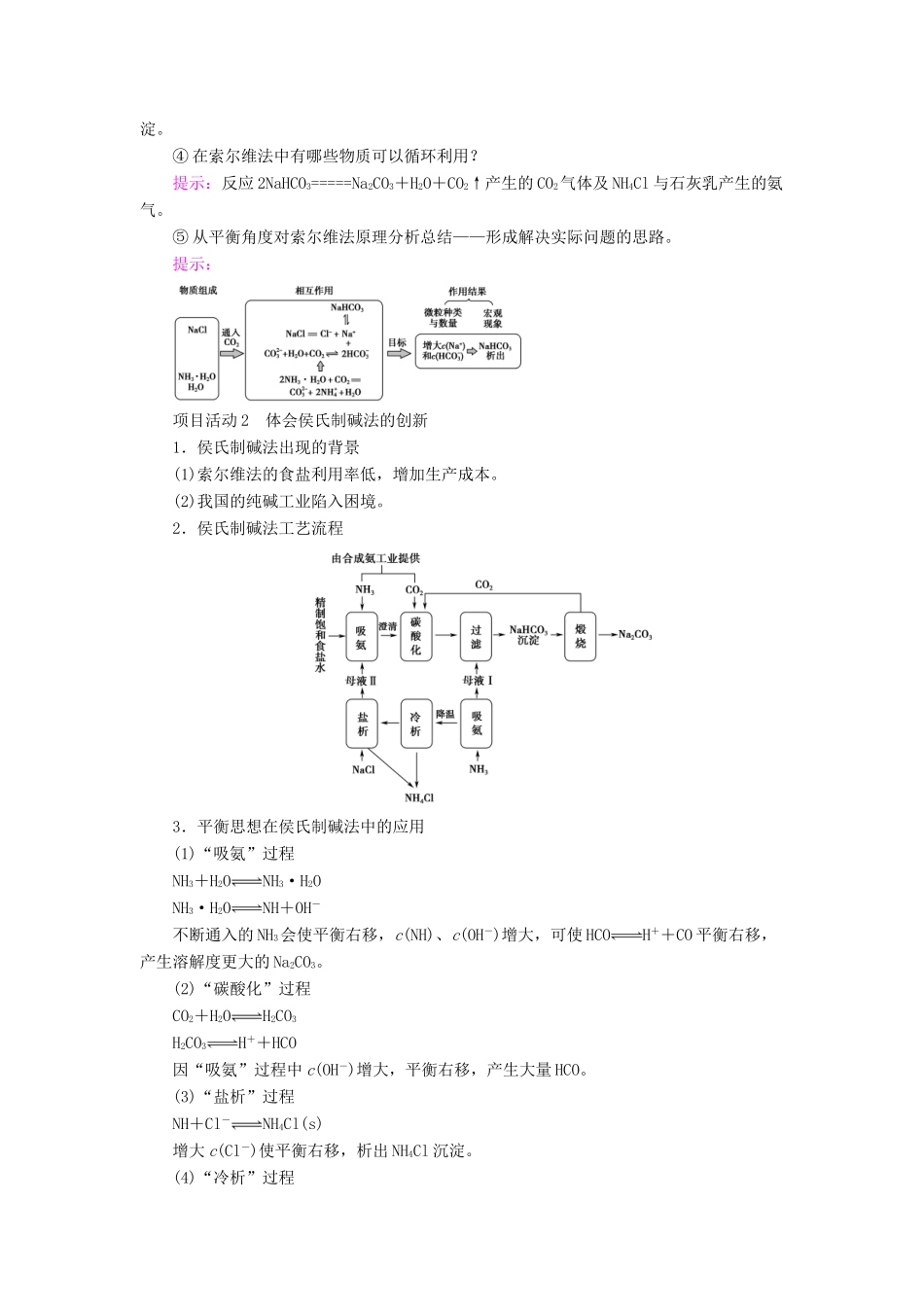
微项目揭秘索尔维制碱法和侯氏制碱法——化学平衡思想的创造性应用1.通过认识制碱工业中复杂的多平衡体系,学会分析溶液中的微粒和平衡,理解平衡之间的相互影响,能根据实际需求选择调控平衡移动的方法
2.通过了解工业制碱的原理,体会化学原理的巧妙应用,了解我国科学家对制碱工业作出的巨大贡献
[必备知识]1.纯碱是重要的基础化工原料,其产量和消费量通常作为衡量一个国家工业发展水平的指标
2.纯碱的用途3.纯碱制法项目活动1解读索尔维制碱法1.关键反应:NaCl+CO2+H2O+NH3===NaHCO3↓+NH4Cl
2.模拟实验(1)实验步骤用如图所示装置模拟索尔维法
锥形瓶中装有碳酸钙粉末,分液漏斗中装有稀硫酸,试管中装有氨盐水,并滴有酚酞溶液
用冰水浴降低试管内的温度
打开分液漏斗,观察二氧化碳通入氨盐水的现象
模拟索尔维法的实验装置(2)实验现象随CO2的不断通入,溶液的红色逐渐褪去后,溶液中出现白色沉淀
(3)问题探究①NaHCO3可溶于水,为什么能得到NaHCO3沉淀
试用化学平衡的原理解释原因
提示:可溶性物质的溶解是存在限度的,当相应离子浓度过大时,可溶性物质也会析出,类似于沉淀溶解平衡
索尔维法通过增大c(Na+)、c(HCO),使平衡Na++HCONaHCO3(s)的Q