第6讲电化学基础[考纲要求]1
理解原电池和电解池的构成、工作原理及应用,能书写电极反应式和总反应方程式
了解常见化学电源的种类及其工作原理
了解金属发生电化学腐蚀的原因、金属腐蚀的危害以及防止金属腐蚀的措施
[学科素养]1
变化观念与平衡思想:认识电化学反应的本质是氧化还原反应,能多角度、动态分析电化学反应,并运用电化学原理解决实际问题
证据推理与模型认知:能运用原电池、电解池模型示意图解释电极及电池反应现象,揭示“放电”“充电”“电解”时现象的本质与规律
科学探究与创新意识:能够发现和提出有探究价值的新型化学电源、环境污染与防治等电化学问题,确定探究目的,设计探究方案,进行实验探究,能根据实验现象总结规律,并勇于提出自己的独到见解
科学精神与社会责任:具有可持续发展意识和绿色化学观念,研究新型高效、绿色化学电源,能对与电化学有关的社会热点问题做出正确的价值判断
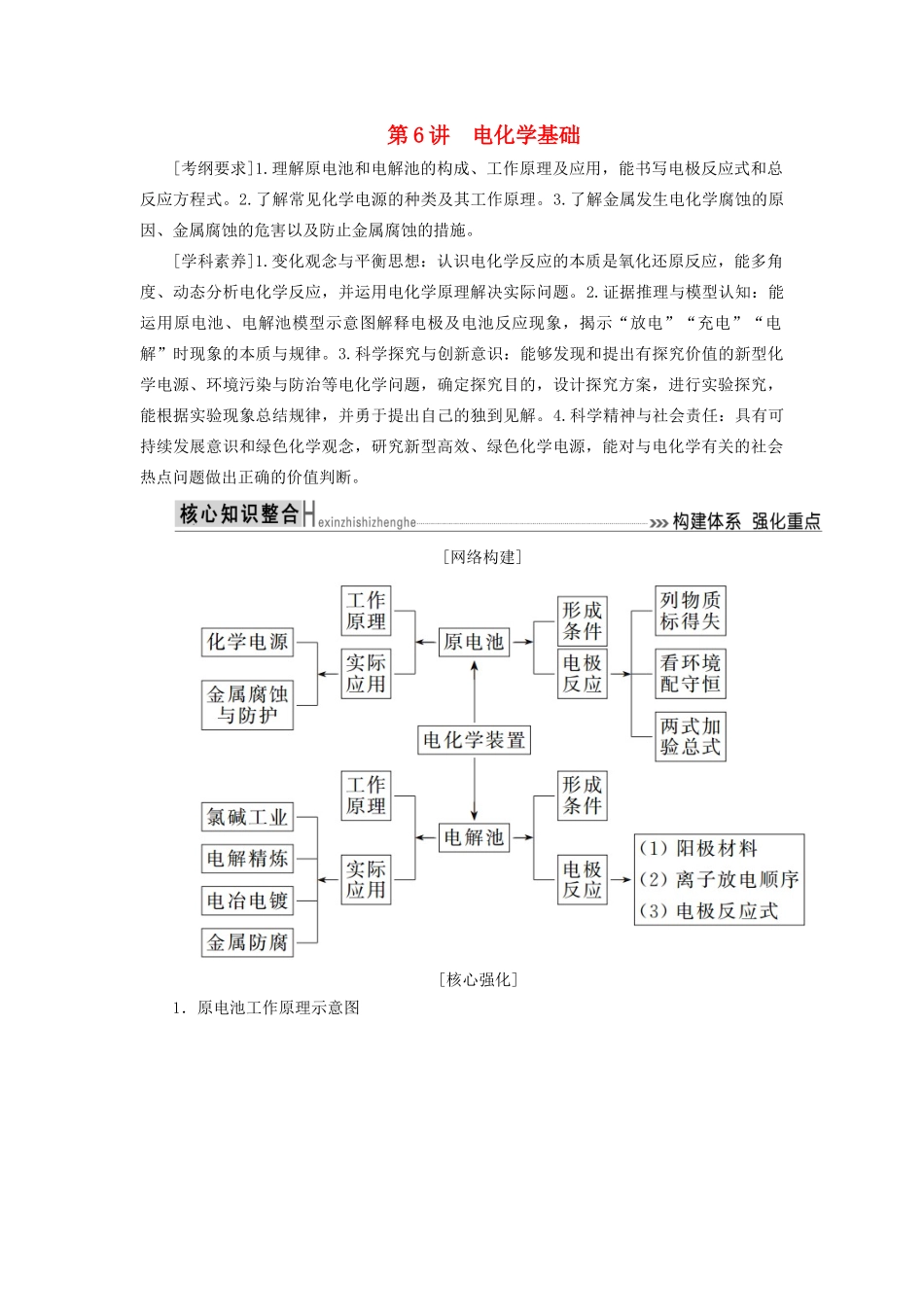
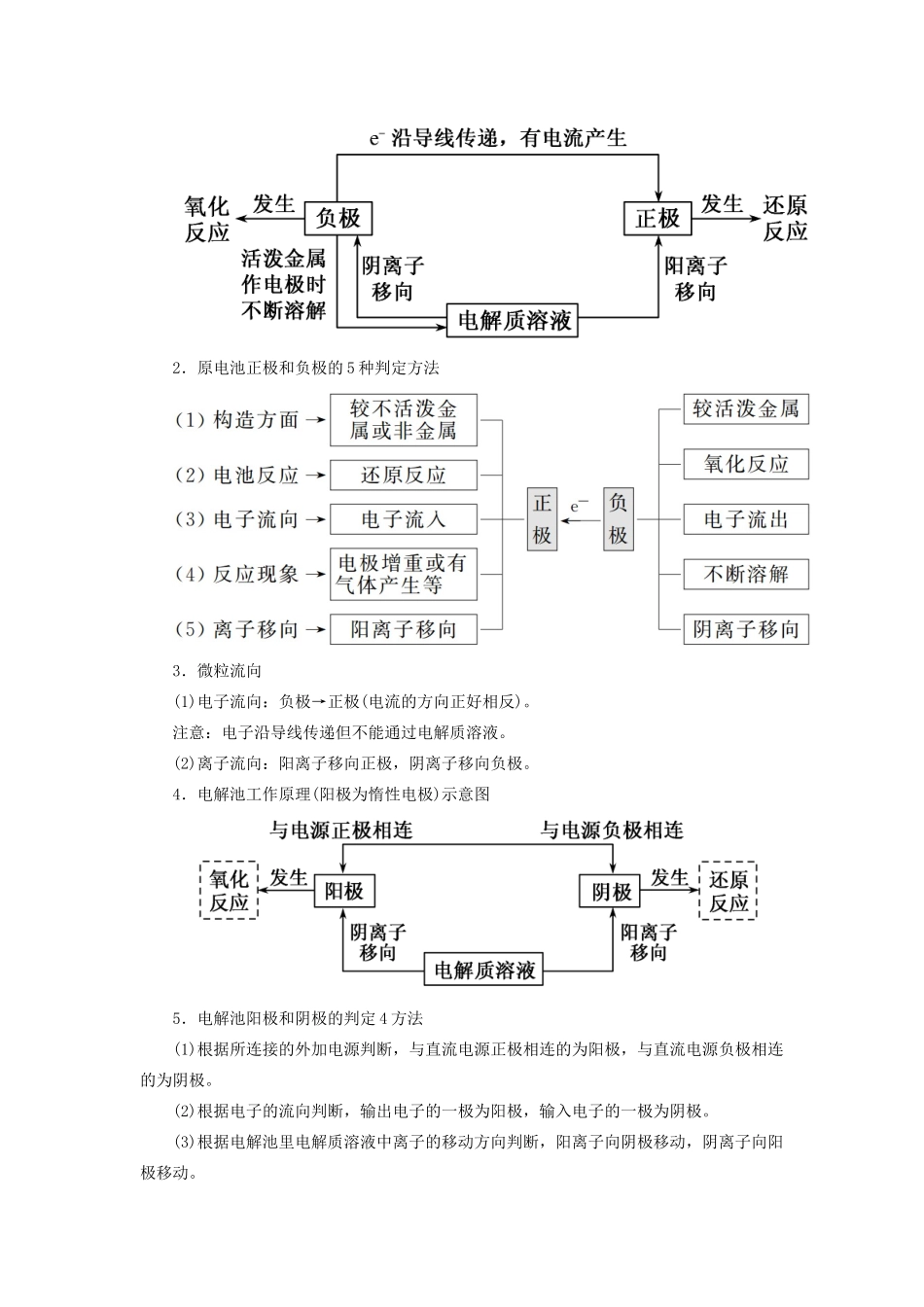
[网络构建][核心强化]1.原电池工作原理示意图2.原电池正极和负极的5种判定方法3.微粒流向(1)电子流向:负极→正极(电流的方向正好相反)
注意:电子沿导线传递但不能通过电解质溶液
(2)离子流向:阳离子移向正极,阴离子移向负极
4.电解池工作原理(阳极为惰性电极)示意图5.电解池阳极和阴极的判定4方法(1)根据所连接的外加电源判断,与直流电源正极相连的为阳极,与直流电源负极相连的为阴极
(2)根据电子的流向判断,输出电子的一极为阳极,输入电子的一极为阴极
(3)根据电解池里电解质溶液中离子的移动方向判断,阳离子向阴极移动,阴离子向阳极移动
(4)根据电解池两极产物判断,一般情况下:①阴极上的现象是:析出金属(质量增加)或有无色气体(H2)放出;②阳极上的现象是:有非金属单质生成(呈气态的有Cl2、O2)或电极质量减小(活性电极作阳极)
6.电解池的电极反应及其放电顺序(1)阳离子在阴极上